 |
TESE
DE LIVRE DOCÊNCIA
IDENTIFICAÇÃO
QUALITATIVA DE VAPOR DE MERCÚRIO CAPTADO DE RESÍDUO DE AMÁLGAMA
DE PRATA, EM DIFERENTES MEIOS DE ARMAZENAGEM
Qualitative
identification of mercury vapor taken up by silver amalgam residues was
performed in several storage media
O grande desenvolvimento tecnológico e o avanço das idéias por que passa o mundo de hoje vêm colocando o trabalho no seu verdadeiro lugar, como útil, necessário e imprescindível, não apenas sob o ponto de vista eminentemente econômico, mas também como fator indispensável à realidade social das comunidades.
Sabe-se que, de início, era o trabalho uma atividade inferior, uma simples modalidade de exploração e, às vezes, uma forma de castigo (tripalium); a capacidade laborativa era quase toda manual, até que o homem começou a utilizar instrumentos cada vez mais aperfeiçoados, desenvolvidos com sua inteligência, para atualmente beneficiar-se da energia atômica como forma de dar ao trabalho seu maior rendimento em favor dos seus semelhantes.
A medida que o trabalho torna-se mais dependente da técnica, o número de acidentes e doenças profissionais aumentam de maneira impressionante.
Sendo o cirurgião-dentista um trabalhador que usa e depende cada vez mais da técnica, está também exposto a um risco muito grande de contrair doenças profissionais e doenças do trabalho ( SAQUY & PÉCORA, 1996).
Dentre os riscos a que o odontólogo está sujeito, diariamente, pode-se citar seus principais agentes, que são: agentes físicos, mecânicos, químicos e biológicos. Dos agentes químicos, a substância que mais causa preocupação aos cirurgiões-dentistas é o mercúrio, restaurações odontológicas com amálgama de prata contendo porcentagens elevadas de mercúrio, são realizadas intensivamente em consultórios odontológicos há mais de 150 anos, BLOCH & SHAPIRO (1982) e GETTLEMAN (1986).
O mercúrio pode ser encontrado no meio ambiente sob várias formas, sendo que na forma metálico é que representa o maior problema de saúde ocupacional, devido a formação de vapores, inodoros e incolores, que possuem grande facilidade de penetração por vias respiratórias.
Os cirurgiões-dentistas estão expostos ao mercúrio metálico quando manipulam o amálgama dental em sua atividade clínica e possivelmente a partir das restaurações de amálgama em seus próprios dentes. Em ambos os casos, segundo HARRIS (1978) e RICHARDS & WARREN (1985), o mercúrio penetra no organismo na forma de vapor de mercúrio metálico.
Desde o primeiro trabalho de GROSSMAN & DANNENBERG (1949), muito se tem publicado nas últimas décadas sobre toxicidade do mercúrio e sobre os riscos decorrentes do emprego deste metal para a saúde dos cirurgiões-dentistas e pessoal auxiliar. Até mesmo clientes, que permanecem por longos períodos em consultórios ou laboratórios onde a manipulação de amálgama é um trabalho de rotina, estão expostos aos efeitos nocivos do mercúrio (RUPP & PAFFENBARGER 1971, BAUER & FIRST 1982, NILNER 1985 e ANDERSON 1988).
A intoxicação por mercúrio utilizado em restaurações de amálgama, que outrora não chamava atenção dos cirurgiões dentistas, passou a ser discutida em virtude dos efeitos deletérios do mercúrio no organismo humano.
No caso específico dos pacientes, as pesquisas estão mais voltadas para os possíveis danos provocados pelo mercúrio emitido de restaurações de amálgama, porém, até ao presente momento os resultados são controversos e pouco esclarecedores, NILSON & NILSSON (1986).
Especialistas afirmam que existe ingestão do mercúrio motivada pelos processos de corrosão e atrição das restaurações de amálgama de prata, ZIFF (1987).
ELIZAUR BENIEZ et al. (1995) observaram que o polimento imediato das restaurações de amálgama promove um aumento significativo nos níveis de liberação do mercúrio, quando comparados com restaurações que receberam polimento mediato e também, que estes níveis diminuem com o decorrer do tempo.
Durante as atividades profissionais do cirurgião-dentista as fontes contaminantes são: gotas derramadas acidentalmente, remoção de excesso de mercúrio, amalgamadores com vazamento, condensadores ultra-sônicos, falhas no sistema de sucção à vácuo quando da remoção de restaurações antigas.
Convém salientar que existem outras formas de contaminação pelo mercúrio, como a que ocorre no momento da preparação do amálgama, pois o mercúrio vaporiza-se à 200C aumentando sua volatilidade a medida que há aumento da temperatura, ampliando-se em até oito vezes, caso a temperatura atinja 500C (WARFVINGE, 1995).
GRONKA et al. (1970) mostraram que a operação que maior risco oferece em relação ao mercúrio é a preparação do amálgama de prata no consultório odontológico, principalmente quando este cai ao chão. Relataram ainda que, quando o ambiente de trabalho do cirurgião-dentista está contaminado, a descontaminação torna-se difícil, embora essencial.
Outra maneira de contaminação seria aquela advinda das raspas de amálgama armazenadas no consultório odontológico (RUPP & PAFFENBARGER, 1971).
Segundo ELIZAUR BENITEZ et al. (1995), o cirurgião-dentista deve armazenar os resíduos de amálgama em recipientes fechados e imersos em água. MAGRO et al. (1994) salientam que todo resto de amálgama deve ser recuperado e armazenado em recipientes fechados e imersos em solução fixadora de radiografia, evitando assim a liberação de vapores de mercúrio.
A liberação de vapores de mercúrio dos resíduos de amálgamas deve ser motivo de preocupação para os cirurgiões-dentistas, estes profissionais, que passam grande parte do seu tempo em seus consultórios, podem estar expostos a grande concentração de mercúrio com o passar do tempo, o que poderia provocar fadiga, esclerose múltipla, arteirosclerose, doença de Alzheimer, nervosismo, irritabilidade, dores de cabeça, instabilidade emocional, (SAQUY & PECORA 1994).
O
objetivo do presente trabalho é indicar, por meio de método
químico, qual a forma adequada de armazenamento e o período
de permanência dos resíduos de amálgama nos consultórios
odontológicos.
Em 1826, TAVEAU, defendia o uso da " Pasta de Prata" para restaurações permanentes. A pasta de prata proposta por TAVEAU constituía-se da simples combinação da prata e mercúrio. Por conveniência, moedas de prata foram gradualmente tomando o lugar da prata purificada. As moedas eram transformadas em limalha e quantidades suficientes de mercúrio eram adicionadas ao material para torná-lo uma pasta ou uma massa maleável. O mercúrio excedente era extraído e a pasta era colocado na cavidade, onde rapidamente endurecia. Assim, graças a genialidade de TAVEAU (1826), que utilizou moedas de prata, as quais continham outros metais (cobre) como matéria-prima para massa de restauração, nasceu o amálgama que foi apresentado ao mundo.
Em 1833, os irmãos CRAWCOUR estabeleceram-se em Nova Yorque e exerceram a Odontologia. Eram dois aventureiros sem instrução, experiência ou habilidade, que divulgavam o uso do amálgama através de uma campanha publicitária sem precedentes. Eles apregoavam que dispunham de um novo tipo de material, muito mais barato que o ouro e que não exigia o tempo e o trabalho gastos no preparo de cavidade para ouro.
Esse novo material promoveu grande controvérsia, pois a Odontologia organizada repudiava e denunciava o uso do amálgama. À frente desta discussão estava a Sociedade Americana de Cirurgiões Dentistas fundada em 1840 pelo Dr. HARRIS, que na mesma época abriu a primeira escola de Odontologia nos Estados Unidos, - Baltimore Dental School. Uma das primeiras resoluções aprovadas pela Sociedade Americana de Cirurgiões Dentistas foi : o uso da pasta mineral lithodeen e todas as substâncias que contivessem mercúrio eram nocivas aos dentes e a todas as partes da boca e que não haveria obturação, na qual o ouro não fosse o material empregado.
Sob a liderança de FLAGG (1870), surgiu o primeiro movimento organizado a favor do amálgama. Este movimento foi marcante pela crença de que o amálgama era um material valioso para restaurações e os relatórios indicativos de sua nocividade à saúde dos pacientes eram mal fundamentados e inverídicos. A maioria das experiências para comprovação da nova tese eram inconclusivas e os dentistas profissionais permaneciam em dúvida quanto à conveniência do uso do amálgama nas restaurações.
BLACK (1900) contribuiu muito para o desenvolvimento da Odontologia e o aperfeiçoamento do amálgama de prata.
Em pesquisa publicada, STOCK (1926) identificou o amálgama odontológico como fonte de vapor de mercúrio, afirmando ainda que " a Odontologia deve evitar completamente o uso do amálgama em obturações ou, pelo menos, não usa-lo quando possível. Não há dúvidas de que sintomas tais como: cansaço, depressão, irritabilidade, vertigem, enfraquecimento da memória, inflamações bucais, diarréia, perda de apetite e catarro crónico, são comumente causados pelo mercúrio, expondo o organismo através das obturações com amálgama".
Em 1935, STOCK apontou uma outra rota de entrada do mercúrio para o corpo, muito interessante. Ele descobriu que parte do vapor de mercúrio liberado pelo amálgama penetrava pelo nariz. Ali era absorvido pela mucosa e rapidamente atingia o cérebro, sendo encontrado no lóbulo e tubo olfativo e na glândula pituitária.
HUNTER (1940) relatou que a constrição progressiva dos campos visuais, frequentemente evoluindo para cegueira, foi registrada repetidamente em quase todas as exposições significativas de seres humanos ao mercúrio.
FRIBERG (1953) citou que exposição crônica ao vapor de mercúrio pode causar proteinúria(excesso de soro proteico na urina, também conhecida por albuminúria) que pode evoluir para uma síndrome nefrótica.
KATSUKI (1957) conclui que distúrbios neurológicos, consistindo principalmente de tremores leves, ataxia (falha na coordenação muscular e movimento irregular) e perda sensorial e visual foram muito freqüentes em observações clínicas de envenenamentos por mercúrio.
FRYKHOLM (1957), após um profundo exame da literatura e numerosos estudos de absorção e excreção do mercúrio, concluiu que a quantidade calculada de exposição ao mercúrio proveniente do amálgama dentário não é suficiente para causar o envenenamento por mercúrio convencionalmente conhecido.
CHEEK (1959) salientou que relatórios clínicos e experimentais sugerem que a exposição prolongada ao mercúrio eleva a atividade simpática.
ROTHSTEIN & HAYES (1960), em experimentos com ratos, demonstraram existir três fases na eliminação do mercúrio, existe uma fase rápida, uma fase mais lenta e uma terceira fase muito mais lenta. Nesta terceira fase o organismo retinha 15% da dose original e foi caracterizada por uma meia-vida de 100 dias.
LIPPMANN (1962) relatou alguns casos curiosos de sensibilidade ao mercúrio de restaurações de amálgama: a) Uma mulher de 35 anos de idade estava pálida e sua condição geral era precária. Ela apresentava uma dentição quase completa, mas a gengiva estava edemaciada com uma coloração vermelho-azulada e a glândula sublingual estava edemaciada. Diversos dentes tinham grandes restaurações de amálgama de prata rico em cobre. O exame de urina mostrou além de alto nível de albumina, traços de mercúrio. Foi estabelecido o diagnóstico de nefrite causada pelas restaurações de amálgama rico em cobre. A remoção de todas restaurações, extração de dentes cariados e o tratamento da gengiva com antinflamatórios resultou em grande melhora. A inflamação desapareceu e a urina depois de 40 dias voltava aos níveis normais de albumina e mercúrio. b) Outro caso relatado foi de uma paciente jovem que precisou de uma restauração e o material escolhido foi o amálgama de prata. Duas horas depois a bochecha da paciente estava vermelha e edemaciada. A restauração foi imediatamente removida e substituída por um cimento. Os sintomas de reação alérgica desapareceram completamente em oito dias.
HAY et al (1963), estudando autópsias humanas, revelaram danos nos cérebros de pessoas que sofreram exposições a compostos de mercúrio orgânico e inorgânico.
DAHAN & ORFALY (1964), estudaram os eletrocardiogramas de 42 vítimas de envenenamento por mercúrio orgânico, sendo que todos apresentaram resultados anormais.
BERGENHOLTZ (1965) publicou dois casos de múltiplos de pólipos gengivais, que desapareceram após remoção das restaurações de amálgama.
YOSHINO et al (1966) estudaram as alterações bioquímicas no sistema nervoso de ratos, resultantes de intoxicação por mercúrio, e concluíram que o envenenamento por compostos de mercúrio podem ser responsáveis pela inibição seletiva de proteínas. STEINWALL & SNYDER (1969), desenvolvendo estudos independentes, confirmaram as observações de YOSHINO (1966), relativas à grande redução de amino-ácidos incorporados ao tecido cerebral, após intoxicação por mercúrio.
Em 1967 MAGOS, em um grupo de experimentos com ratos, demonstrou que o vapor de mercúrio, em sua forma elementar, pode alcançar o cérebro.
JOSELOW (1968), pesquisando 50 consultórios dentários, encontrou em 14% destes concentrações de mercúrio no ar acima dos limites de tolerância estabelecidos. Os cirurgiões dentistas expostos ao metal apresentavam valores de mercúrio na urina superiores ao limite de tolerância biológica.
COOK & YATES (1969) relataram um caso de intoxicação fatal de uma assistente dental, uma senhora de 42 anos que trabalhou pelo menos por 20 anos, e durante este tempo manipulava regularmente o mercúrio usado para o amálgama. Ela estava completamente bem quando começou subtamente a vomitar, apresentando dores na região lombar direita do abdômen, edema na face e nas pernas, passando a urinar escuro. A persistência desses sintomas por seis dias resultou em sua internação hospitalar. Foi feito um diagnóstico de nefrite e o tratamento iniciado com esteróides e diuréticos. Contudo sua condição geral piorou rapidamente, passando a apresentar deficiência renal aguda, vindo a falecer poucos dias após.
Em 1969, DJERASSI & BEROVA descobriram que 16,1% dos indivíduos submetidos aos testes, apresentaram reação positiva de hipersensibilidade ao mercúrio e seus componentes. Os autores usaram 60 pessoas, como grupo de controle, que não possuíam qualquer restauração de amálgama em suas bocas. Os controles (pessoas sem amálgama) foram submetidos à mesma série de testes aplicados nas outras 180 pessoas participantes do estudo. Ninguém do grupo controle teve reação positiva aos testes. Por outro lado, 16,1% dos outros pacientes testados tiveram reação positiva. Dos pacientes portadores de restaurações de amálgama há mais de 5 anos, 22,5% apresentaram reação positiva.
TEIXEIRA et al (1970) analisaram quantitativamente a emissão de vapor de mercúrio das superfícies das restaurações com amálgama. O método baseia-se na reação do vapor de mercúrio com o sulfeto de sêlenio aplicado a uma folha de papel sulfite, cujo resultado é a formação de manchas de sulfeto de mercúrio na superfície do papel impregnado. Executaram uma série de 8 corpos de prova em placas de acrílico e 4 restaurações de classe V em dentes recém-extraídos, utilizando liga de amálgama de corte fino. Após a condensação, metade dos corpos de prova e das restaurações foi submetida à brunidura com o auxílio de um brunidor número 6 de Hollenback. O controle era constituído de cavidades preenchidas com limalha misturada com cimento de fosfato de zinco, ao invés de mercúrio. Os corpos de prova eram cobertos com papel sulfite no qual era aplicado o sulfeto de selênio, tendo uma folha de papel filtro interposta entre ambos, e colocados em estufa a 37 graus. Após 12 horas de exposição, os papéis eram removidos para exame. Os corpos de prova eram recolocados na estufa para armazenamento, em temperatura controlada, e 24 horas após a condensação eram polidos e novamente submetidos ao teste. Verificaram que os corpos de prova brunidos apresentaram menor emissão de vapor de mercúrio, particularmente nas áreas marginais. Após sofrerem polimento, os corpos de prova reduziram acentuadamente a intensidade de impregnação. Contudo, o efeito da brunidura foi novamente evidente, uma vez que os corpos de prova brunidos após a escultura tiveram pequena ou nenhuma impregnação após polimento
ROTHSTEIN (1971) afirmou que para exposição por longo prazo ao vapor de mercúrio, o órgão que primeiro apresenta distúrbios de ordem funcional parece ser o sistema nervoso central. Os efeitos tóxicos são produzidos após o organismo converter ou transformar o elemento vapor de mercúrio em íons mercúrios.
Segundo SNYDER (1972), os sintomas de envenenamento por mercúrio no homem incluem distúrbios psíquicos e comportamentais.
BUCHWALD (1972), além da determinação do mercúrio presente na atmosfera de trabalho e na urina dos profissionais expostos, verificou que a contaminação das mãos, consequente do contato com o mercúrio metálico ou amálgama, é uma maneira significativa de introdução do metal no organismo.
CHAN & SVARE (1972) procuraram observar se a emissão de vapor de mercúrio poderia ser afetada pelo tipo de liga e técnica de acabamento. Quatro tipos de ligas foram avaliadas: corte micro, corte micro extra-fina, esferoidal e mistura de esferoidal com corte micro. Os amálgamas foram condensados em cavidades circulares de bloco de "plexiglass" com 8 mm de diâmetro por 3 mm de profundidade. Decorridas 24 horas da escultura, as superfícies do amálgama eram brunidas ou polidas. Para detectar a emissão de vapor de mercúrio, empregaram o método de NORDLANDER, modificado por TEIXEIRA et al (1970). Os resultados mostraram que o amálgama tipo corte micro emitiu uma quantidade maior de mercúrio que os demais, para os corpos de prova esculpidos e brunidos, durante 72 horas. No período inicial de 24 horas, o amálgama esferoidal emitiu menor quantidade de vapor de mercúrio na superfície esculpida, em relação aos amálgamas de mistura esferoidal com corte micro e de corte micro extra-fina. Em relação aos brunidos e esculpidos não foi encontrada diferença estatística. A emissão de vapor de mercúrio foi maior nas margens para todas as condições em estudo e diminuiu com o tempo, não mais sendo detectada após 5 dias.
MANDETTA (1972) estudou a influência da brunidura no conteúdo de mercúrio na superfície do corpo de prova, preparado com limalhas de corte fino (pré-amalgamada) e esferoidal (sem zinco), após a escultura. Analisou quantitativamente o mercúrio da superfície dos corpos de prova e concluiu: 1- Os corpos de prova com a idade de 5 minutos apresentaram o mesmo conteúdo de mercúrio que os corpos de prova com a idade de 24 horas; 2- A brunidura da superfície do corpo de prova após a escultura, para todas as cargas aplicadas, tem a tendência de diminuir o conteúdo de mercúrio da região superior do corpo de prova. Embora a diminuição do conteúdo de mercúrio seja estatisticamente significante para a carga de 2 Kg, talvez na prática não tenha significado clínico. Em síntese: a brunidura tem a tendência de diminuir o conteúdo de mercúrio da superfície do corpo de prova e não de aumentá-lo; 3- Os corpos de prova obtidos de limalha de corte fino apresentaram menor conteúdo de mercúrio que os feitos de limalha esférica; 4- Os corpos de prova estudados apresentaram maior quantidade de mercúrio na região posterior, menor conteúdo de mercúrio na região inferior e teor intermediário na região média; 5- Houve diminuição nítida do conteúdo de mercúrio na região superior do corpo de prova na idade de 24 horas, com aumento nas regiões média e inferior. Esta variação ocorreu pela difusão do mercúrio da região superior para as camadas mais inferiores; 6- Algumas interações mostraram-se estatisticamente significantes, o que demonstra que certos fatores podem ter influência recíproca.
A American Dental Association (1974), após determinação do teor de mercúrio em consultórios odontológicos, em vários estados americanos, verificou que 37% dos ambientes possuíam concentração acima do limite permissível, estabelecido pela American Conference of Governamental Industrial Hygienistis, ou seja, de 0,05 microgramas de mercúrio inorgânico por metro cúbico.
FREDEN (1974), afirmou que reações inflamatórias locais, induzidas por restaurações de amálgama, foram observadas em tecidos gengivais.
WANNAG & SKJAERASEN (1975), para investigar os perigos da exposição ao mercúrio elementar, estudaram dois grupos de mulheres grávidas, o primeiro grupo de dentistas e o segundo grupo de mulheres não expostas aos vapores de mercúrio. Os resultados mostraram que, a quantidade de mercúrio no sangue de mães e bebês no nascimento foi similar. O grupo exposto teve a quantidade de mercúrio na placenta e nas membranas fetais aumentadas, os autores acreditam que o acúmulo de mercúrio nesses órgãos deve servir como proteção ao feto contra a exposição ao mercúrio. No grupo exposto a concentrações de mercúrio inferiores à normalidade, não foi encontrado mercúrio na placenta e na membrana fetal. Os autores concluem afirmando que, a presença de mercúrio na placenta e membrana fetal poderia servir como indicador biológico a essa exposição.
Em 1975, BRUN publicou os resultados de um estudo no qual 1000 pacientes com dermatite de contato foram testados para avaliação de hipersensibilidade ao mercúrio, apresentaram resultado positivo ao teste 11,3% dos pacientes.
MANTYLA & WRIGHT (1976) afirmaram que nos Estados Unidos, pelo menos 10% dos consultórios apresentaram níveis de vapor de mercúrio no ar mais elevados que o limite máximo, de 0,05 mg/m3 de ar, estabelecido para a segurança numa exposição de 8hs/dia.
Um estudo realizado, por WHITTE & BRANT (1976), em estudantes de Odontologia avaliou a incidência de hipersensibilidade ao Hg. Notou-se que a mesma aumentava com a exposição ao amálgama de prata durante os quatro anos da faculdade. Verificou-se que os resultados positivos dos testes alérgicos aumentaram significantemente nos indivíduos de último ano (10,8%) quando comparados aos calouros (2%), apesar de que nenhum deles apresentavam sintomas devido a essa hipersensibilidade.
GERSTNER & HUFF, em 1977, concluíram que os sintomas de envenenamento por mercúrio são um reflexo dos danos causados tanto no sistema nervoso central como no sistema nervoso periférico.
BOYER & CHAN (1977) estudaram o efeito da brunidura na emissão de vapor de mercúrio das superfícies de amálgamas esculpidos e brunidos, obtidos de ligas convencionais com partículas esferoidais, utilizando um detector de vapor de mercúrio. Após a trituração, o amálgama foi condensado manualmente em cavidades de 0,78 cm de diâmetro e 0,15 cm de profundidade. Parte das amostras foi esculpida com uma lâmina de aço afiada e outra parte foi brunida, com leve pressão (12g), 12 minutos após. Foram utilizadas 4 amostras para cada acabamento, a temperatura ambiente, nos tempos de 5, 15, 30, 45 e 60 minutos. Os autores concluíram que, a maior variação na emissão de vapor de mercúrio ocorre entre 5 e 15 minutos após a brunidura e eram maiores nos amálgamas brunidos. Este fato sugere afloramento de mercúrio à superfície.
VANDENBERGE et al (1977), ao analisarem o teor de mercúrio no sangue de elevado número de cirurgiões dentistas e auxiliares diretos, verificaram um índice superior a 50% de indivíduos com valores anormais.
SILVA & GANDINI (1978), após levantamento bibliográfico, puderam concluir que existe risco bastante sério na contaminação do pessoal odontológico (dentista e auxiliares) e pequeno ou nenhum risco para os pacientes. Entretanto, se medidas de higiene forem tomadas, o risco praticamente desaparece, de modo a deixar o nível de mercúrio no ar e na urina dentro dos valores considerados normais.
KELMAN (1978) relatou níveis maiores de mercúrio na urina de auxiliares odontológicos (38 microgramas por litro) que em cirurgiões dentistas (22 microgramas por litros).
Pesquisa realizada por TILL & MALY (1978), evidenciou níveis de mercúrio superiores a 1200 microgramas por grama de tecido nas pontas de raízes de dentes que possuíam restaurações de amálgama e ouro. Algumas centenas de microgramas de mercúrio por grama de tecido foram encontrados nas pontas de raízes de dentes com restaurações somente de amálgama. Os autores afirmaram ainda que, os níveis registrados aumentaram com o tempo e que o mercúrio não era originário da alimentação.
GOLDMAN & BLACKBURN (1979) descreveram experimentos com ratos, para os quais foram ministradas doses de mercúrio e de iodo radioativo. O objetivo era verificar se o mercúrio afetaria a habilidade das glândulas tireóides em absorver o iodo. Nos ratos em que foram aplicadas doses orais de mercúrio, em um período de 90 dias, houve sinais de envenenamento por mercúrio, junto com a redução de absorção do iodo radioativo. Houve também queda na taxa de secreção de hormônios da tiróide. Após 90 dias adicionais, durante os quais os ratos não sofreram exposição ao mercúrio, verificou-se que não houve recuperação na depressão das funções da tireóide, concluindo-se assim que eram danos permanentes e irreversíveis.
Estudos morfológicos, comportamentais e fisiológicos de REUHL & CHANG (1979) mostraram que o mercúrio exerce efeito prejudicial ao sistema nervoso de fetos, mesmo em doses consideradas não-tóxicas para adultos.
POPESCU (1979) observou em linfócitos, cultivados de seres humanos expostos ao mercúrio, altas freqüências de aberrações cromossômicas.
GOODMAN & GILLMANS (1980) afirmaram que o envenenamento pela inalação de vapores de mercúrio é caracterizado por gosto metálico, estomatite, mau hálito, gengivite e salivação excessiva. Processos de necrose do alvéolo, perda de dentes e descoloração nas margens gengivais podem aparecer mais tarde.
LARINI & SALGADO (1981), considerando o valor de normalidade de 10 g/1000 ml de urina, analisaram amostras de urina de vinte e dois cirurgiões dentistas da cidade de Araraquara (SP), verificando que 72,7 por cento destes profissionais apresentavam teores de mercúrio acima do valor de normalidade.
ANCONA et al (1982) relataram casos de dermatite alérgica entre membros da equipe odontológica. Os sinais e sintomas ocasionalmente relatados e relacionados às restaurações de amálgama são: dermatite facial, algumas vezes com áreas eritematosas, urticárias e líquen plano.
FINNE (1982) descobriu que em um grupo de 29 pacientes com líquen plano oral (doença inflamatória) 62% reagiram de forma positiva ao teste de hipersensibilidade ao mercúrio. O interessante no estudo é que em 4 dos pacientes todas as restaurações foram removidas e substituídas por ouro ou resinas compostas, com os seguintes resultados: as lesões, em 3 desses pacientes, cicatrizaram completamente depois de um período de observação de 1 ano e o último caso registrou uma considerável melhora.
WILSON & WILSON (1982) estudaram o vapor de mercúrio provocado durante a trituração do amálgama e na abertura da cápsula, de diversos modelos de amalgamadores. A mensuração foi realizada por um espectrofotometro de absorção atômica. Os autores concluíram que o vapor de mercúrio vazado durante a trituração com cápsula disponível é muito pequeno, quando da abertura da cápsula, o resultado do vazamento não foi maior que o limite recomendado.
Em 1983, NEBENFUHER testou 1538 pacientes internos (780 homens e 758 mulheres) com uma série de testes de alergia rotineiros, incluindo mercúrio. Descobriu-se que 9,6% das pessoas testadas eram alérgicas ao mercúrio (91 mulheres e 57 homens).
MOBACKEN (1984) relatou que em um grupo de 67 pacientes portadores de liquen plano oral, 16% reagiram positivamente ao teste de alergia ao mercúrio. Descobriram que a maioria das reações eram devidas ao elemento mercúrio.
Segundo MAREK (1984), após a mastigação de duas horas por dia serão liberados do amálgama convencional fresco 500-700 microgramas de mercúrio por centímetro cúbico de restauração, isto é, 5-7 miligramas de mercúrio por 10 centímetros quadrados de superfície.
NALEWAY et al (1985) encontraram uma média de 14,2 microgramas de mercúrio por litro de urina em 4272 cirurgiões dentistas, entre 1975 e 1983. Em 4,5% das amostras os níveis estavam acima de 50 microgramas por litro e em 1,3% acima de 100 microgramas por litro. A variação se deve provavelmente às técnicas de colheita, metodologia e variação na exposição ocupacional.
HURSH et al (1985) propuseram o emprego de técnica de diluição isotópica, com mercúrio radioativo, associada à administração do quelante DMPS (dimercaptopropano sulfonato), para se predizer o conteúdo renal de mercúrio. Conforme os autores, tal teste pode servir para avaliação de exposição ocupacional excessiva a vapores de mercúrio.
Em 1985, VIMY & LORSCHEIDER publicaram um estudo clássico que, ao invés de medir o ar exalado como em outros estudos , mediu as concentrações de mercúrio no ar intra-oral antes e após a mastigação por 10 minutos, de goma de mascar. Esse estudo também revelou que, uma vez concluída a mastigação da goma, leva-se 90 minutos para que a leitura do vapor de mercúrio intra-bucal retorne aos níveis pré-estímulo. Estes dados foram então, extrapolados para três refeições e dois lanches diários e desenvolvidas uma série de fórmulas que calculavam o potencial acumulado da elevação na carga total de mercúrio no organismo, que estaria diretamente vinculada às restaurações de amálgama. Os autores fazem a seguinte afirmação: " Estas dosagens de mercúrio provenientes do amálgama atingiram "18-fold", que é o limite estabelecido, em vários países, para a exposição diária ao mercúrio, de todas as fontes ambientais. Os resultados demonstraram que a quantidade do elemento mercúrio liberado do amálgama excede ou atinge os valores limites adotados internacionalmente para a exposição ambiental ao mercúrio. Conclui-se que o mercúrio originado do amálgama dentário constitui-se na parte principal da dose diária total".
EMLER & CARDONE (1985) realizaram estudos usando pacientes pediátricos com idades de 5 a 12 anos, estas crianças registraram baixa exposição ao mercúrio, pouco consumo de peixes, e nenhuma ingestão de bebidas alcoólicas (pontos que afetam a forma como o organismo se comporta em relação ao mercúrio). Os níveis de mercúrio foram comparados antes e depois da inserção da restauração de amálgama. O trabalho conclui com esta afirmação: "Demonstrou-se uma correlação causal entre as restaurações de amálgama e a exposição ao vapor de mercúrio. A mastigação elevou a evaporação de mercúrio em amálgamas instalados há uma semana".
MILLER (1985) desenvolveu um estudo na Escola de Odontologia da Baylor University em Dallas, Texas, envolvendo 171 estudantes voluntários (51- do primeiro ano, 52- do segundo ano, 37- do terceiro ano e 31- do quarto ano). O autor descobriu uma significativa correlação entre o número de amálgamas e a incidência de hipersensibilidade ao mercúrio. Outro aspecto interessante desse estudo foi a taxa de hipersensibilidade ao mercúrio registrada nos alunos do primeiro ao quarto ano, que foi de 31%, 27%, 32% e 39%, respectivamente.
Segundo GOYER (1986), um trabalhador sujeito a uma concentração média constante de vapores de mercúrio pode atingir um estado de equilíbrio dinâmico após cerca de um ano de exposição, estabelecendo-se uma correlação entre os níveis de mercúrio no ar, sangue e na urina.
SALGADO (1987) confirmou que a exposição ocupacional pode resultar em níveis urinários de mercúrio superiores aos da população não ocupacionalmente exposta, sendo que os profissionais mais jovens apresentavam níveis mais elevados de mercúrio na urina do que profissionais mais antigos, sugerindo a necessidade de as escolas melhorarem a formação dos alunos quanto a medidas preventivas de contaminação.
Uma das documentações mais completas sobre exposição de mercúrio total proveniente do amálgama dental e sua absorção foi publicada por HAHN et al (1989) e VIMY et al (1990). O mercúrio radioativamente marcado de 12 restaurações feitas em ovelhas, foi encontrado em todo o corpo do animal, sendo que foram feitas medidas em tecidos específicos. Esta investigação confirmou as 3 vias principais de absorção do mercúrio: pulmão, trato gastrointestinal e o tecido ósseo do maxilar. Após um mês, o conteúdo de mercúrio total do rim era igual a 1,86 miligramas e do fígado igual a 0,77 miligramas. Também o cérebro, glândula pituitária, tireóide, pâncreas e ovários mostraram evidências de acúmulo de mercúrio, proveniente do amálgama dental. A eliminação diária de mercúrio estava acima de 9 miligramas em 2000 gramas de fezes.
Estudos de MANDEL (1991) concluíram que os organomercuriais, usados no passado como diuréticos, e o mercúrio inorgânico em altas concentrações, usado no tratamento de pele, têm sido associados com a chamada glomerulonefrite imunologicamente mediada. Porém, influências do amálgama sobre a glomerulonefrite não são confirmadas.
Avaliando a possível relação entre restaurações de amálgama e a situação imunológica, MACKERT (1991) comparou subclasses de linfócitos em 21 pessoas com, e 16 sem restaurações de amálgama, não encontrando diferença no número de células T, B e de linfócitos granulares, que incluem células "killer". Concluiu-se que não existem indicações de que as restaurações de amálgama sejam responsáveis pela diminuição da imunocompetência.
NASCIMENTO et al (1991) testaram a fuga de mercúrio ocorrida durante a trituração mecânica do amálgama, testando diferentes cápsulas. Os resultados permitiram concluir, com segurança, que nenhuma das cápsulas testadas pode ser considerada hermética.
BJORKMAN & LIND (1992) estudaram os fatores que influenciam a evaporação de mercúrio nas restaurações de amálgama, em onze pacientes voluntários, antes e após a mastigação de chicletes. O ar da cavidade bucal foi aspirado por um minuto, e imediatamente analisado com detector de mercúrio. Verificou-se que, após a mastigação com chiclete, o vapor de mercúrio aumentou no interior da cavidade oral.
HOLLAND (1993) determinou a liberação do vapor de mercúrio por sete amálgamas diferentes, que foram expostos para induzir a corrosão pelo contato galvânico, com restaurações metálicas fundidas em ouro. O autor verificou que não houve diferença significativa no total de mercúrio liberado entre os amálgamas convencionais e os de alto teor de cobre.
Segundo SURMONT & ENODY (1993), há um consenso quanto ao respeito que se deve ter em relação ao meio ambiente, quando relacionado a redução do lixo tóxico do consultório odontológico. Uma das preocupações do cirurgião-dentista deve ser a redução do fluido de amálgama, o qual contém mercúrio, começando pela instalação de um dreno para escoar o amálgama. Os maiores pedaços de amálgama devem parar no filtro, os autores concluem que o uso de materiais alternativos e técnicas apuradas ajudarão a reduzir os restos de amálgama encontrados no esgoto dos consultórios.
VALE (1993) estudou morfológica, morfométrica e estereologicamente as alterações epiteliais, causadas pela administração de mercúrio, nas regiões dorsal anterior, dorsal posterior e ventral da língua de fetos de ratas que receberam a droga durante a prenhez. Os resultados obtidos neste trabalho demonstraram que o mercúrio provoca malformações fetais como morte e reabsorção. A incidência de malformações e mortes fetais está diretamente relacionada ao aumento da dose de mercúrio. O epitélio língual mostrou um quadro de aumento de tecido com aumento de número de células para as regiões dorsais anterior e posterior e diminuição da espessura epitelial com menor número de células para a região ventral.
BJORKMAN et al (1994) analisaram a concentração de mercúrio e selênio, em frações de tecido de rim humano examinados em sete casos de autópsias. No córtex do rim de um dentista, somente 3% do total de mercúrio foi encontrado. Este estudo comprovou resultados prévios obtidos com animais, indicando que o mercúrio no rim humano poderia ser depositado com diferentes solubilidades.
MAGRO et al (1994) discorreram sobre a segurança no uso do mercúrio nas restaurações de amálgama. As eventuais reações alérgicas ou ocorrências tóxicas a esse metal são apresentadas, bem como os procedimentos para sua higienização.
WARFVINGE (1995) relatou o caso de uma cirurgiã-dentista de 30 anos de idade que foi exposta ao vapor de mercúrio por aproximadamente um ano, nenhum efeito tóxico foi notado. Durante e depois da exposição, amostras de urina foram regularmente coletadas para análise do mercúrio. O mais alto valor durante este período foi de 60 microgramas Hg/l de urina. A concentração de mercúrio no ar foi também medida em 840 microgramas/m3 (o limite para exposição ocupacional é de 0,50 microgramas/m3). A cirurgiã dentista engravidou e durante a gravidez sua urina foi analisada, verificando-se uma concentração de 18 microgramas Hg/l. O exame do ultra-som do feto com 20 semanas de gestação mostrou uma suave hidronefrose bilateral. Com 32 semanas de gestação a hidronefrose foi sanada. A dentista deu a luz a um menino com peso normal, o qual até a elaboração do trabalho apresentava 2 anos de idade estando clinicamente normal.
STOZ et al (1995) afirmaram que dentes com restaurações de amálgama são suspeitos de terem causado diversas moléstias, em pacientes grávidas. Exame de sangue foi realizado 45 dias depois do conhecimento da gravidez, depois do nascimento, as crianças e as placentas foram examinadas para verificação da concentração de mercúrio. Comparou-se 121 mulheres com restaurações de amálgama, com 19 mulheres sem restauração de amálgama. A superfície da restauração de amálgama foi medida em mm2 em cada caso. Em 58 mulheres os dentes restaurados continham o mercúrio suplementar. Enquanto nas placentas foi encontrado uma concentração 10 vezes maior de mercúrio, mas baixa correlação para as superfícies de amálgama. As concentração de mercúrio nos exames de sangue das mães e das crianças não tiveram correlação com as restaurações de amálgama. Os autores afirmaram que, o aumento do nível de mercúrio sem correlação com as restaurações, mostra a influência de outros fatores ambientais.
STOZ et al (1995) realizaram estudos para medir a contaminação de mercúrio de mães e filhos, foram examinados 185 mulheres com dentes restaurados com superfície de 0 a 780 mm2. O valor de mercúrio das mães e filhos, por um tempo, mostrou uma correlação significativa com média de valores de 0,4 a 0,5 microgramas de mercúrio. Obviamente, a placenta tinha uma retenção 10 vezes maior de mercúrio, e uma baixa correlação com as superfícies de amálgama. Não houve relação entre o nível de mercúrio no sangue das mulheres e das crianças quando comparados com o tamanho da superfície das restaurações, oposto a isto, o alto consumo de peixe contaminado elevou o nível de mercúrio no sangue do cordão umbilical, mesmo nas crianças de mães sem restaurações de amálgama. Outras pessoas foram expostas a outras condições de contaminação, como por exemplo através do trabalho (atendente de consultório dentário) ou morando num ambiente contaminado. Sintomas da doença como: dor de cabeça, alergia e equizemas surgiram naqueles pacientes que tinham restaurações de amálgama tanto quanto naqueles do grupo sem restaurações de amálgama. Todas as mulheres deram a luz a crianças saudáveis. Os autores concluíram que, com toda cautela necessária que o assunto merece, não se justifica entrar em pânico.
ELIZAUR
BENITEZ et al (1995) analisaram
in vitro os níveis individuais
de liberação de mercúrio em amálgamas confeccionados
com liga do tipo convencional e de alto teor de cobre em função
dos momentos da realização do polimento e tempo. Foi utilizado
o método de Espectrofotometria de Absorção Atômica.
Verificou-se, entre outras observações, que o polimento imediato
exerce um efeito significativo nos níveis de liberação
de mercúrio dos amálgamas estudados, quando comparados com
aqueles que receberam polimento mediato. Observou-se também que
esses níveis diminuem com o transcorrer do tempo.
Com base na revisão da literatura, sabe-se que o amálgama odontológico emite vapor de mercúrio, e que os resíduos desse material são armazenados em consultórios odontológicos.
O presente trabalho propõe-se a:
1º. Apresentar um método químico que detecta, com facilidade, a presença de mercúrio no ar.
2º. Verificar qual substância química impede a passagem do vapor de mercúrio dos resíduos de amálgama armazenados no consultório odontológico.
1. Preparo da Solução de Cloreto de Paládio reveladora da presença de mercúrio.
Pesou-se 1 grama de cloreto de paládio (Merck) em um bequer de 100 ml, adicionou-se álcool etílico 96% até completar o volume total de 100 ml de solução. A solução alcóolica de 1% de cloreto de paládio foi em seguida colocada em um frasco de vidro de cor âmbar e guardado em local isento de luz, até momento do uso.
2. Método Químico para identificação do vapor de mercúrio.
Para a identificação do vapor de mercúrio, adaptou-se o método proposto por FEIGL & ANGER (1972), que utiliza a reação química de substituição entre o cloreto de paládio e o mercúrio metálico. A solução de cloreto de paládio a 1% foi colocada em uma "tira" de papel de filtro Watman com 2 cm de comprimento por 0,5 cm de largura. A seguir, a "tira" de papel contendo cloreto de paládio era seca no interior de um desumidificador contendo grânulos de sílica, de modo a evitar contaminação com o ar do ambiente.
Após
secagem da fita de papel impregnada com cloreto de paládio, realizou-se
um "spot-test" para confirmar a validade do método. A fita de papel
foi colocada na parte superior de um tubo de ensaio, que continha mercúrio
em seu interior. Assim, a fita de papel de cor amarelo claro (cloreto de
paládio) tornou-se, imediatamente, preta (Figura 1). A mudança
de cor evidencia que o vapor de mercúrio atingiu o cloreto de paládio
e promoveu a seguinte reação química:
PdCl2
+ Hg0® HgCl2
+ Pd0
FIGURA 1. "Spot test": A- Papel de filtro com cloreto de paládio revelado pelo vapor de mercúrio; B- Papel de filtro com cloreto de paládio não revelando a presença do vapor de mercúrio.
3. Substâncias químicas utilizadas para impedir a passagem do vapor de mercúrio dos resíduos de amálgama.
Testou-se as seguintes substâncias químicas, como meio de impedir a passagem do vapor de mercúrio emitido pelos resíduos de amálgama:
a) Solução de EDTA - pH=7,3 (Etilenodiaminotetracetico sal dissódico).
b) Solução de EDTA - pH=6,0 (Etilenodiaminotetracetico sal dissódico).
c) Álcool 96%.
d) Água.
e) Fixador Radiográfico(Kodak).
f) Propilenoglicol.
g) Óleo Vegetal (soja).
h) Óleo Mineral.
i) Revelador Radiográfico (Kodak)
Esses líquidos, na quantidade de 4 mililitros, eram colocados em um tubo de ensaio, que já continha previamente 1 g. de resíduos de amálgama (Figura 2).
FIGURA 2. Tubo de ensaio contendo: A- Líquido testado; B- Resíduos de Amálgama.e C- Rolha própria.
A seguir, o tubo de ensaio era fechado com uma rolha de cortiça, perfurada em seu centro, por onde passava um tubo de 0,5 mm de diâmetro, com forma de "S" (Figura 3).
FIGURA 3. Dispositivo senoidal: A- Comunicação entre as extremidades (0,5 mm).
Na outra extremidade do tubo de vidro era colocado, de modo invertido, outro tubo de ensaio, que continha uma fita de papel de filtro Watman seca, previamente impregnada com solução de cloreto de paládio. Assim, o dispositivo montado impedia o contato entre os resíduos de amálgama e a fita de papel contendo a substância reveladora da presença do vapor de mercúrio. Deste modo, entre o resíduo de amálgama e o papel indicador havia a camada de líqüido e a camada de ar. Esse conjunto pode ser visto na Figura 4.
FIGURA 4. Conjunto contendo: A- Tubo de ensaio com resíduos e líquido testado; B- Dispositivo senoidal e C- Tubo de ensaio contendo o papel de filtro impregnado com cloreto de paládio.
Os resíduos de amálgama utilizados no experimento foram coletados na Clínica da Faculdade de Odontologia de Ribeirão Preto da Universidade de São Paulo, no momento das esculturas de restaurações. Esse amálgama era composto de limalha da marca Velvaloy (SS White) e mercúrio (Wilcos do Brasil Ltda), misturados em um aparelho, amalgamador Dosamat - da marca Dabi Atlante -, na proporção de 1:1 (Figura 5).
FIGURA 5 Amalgamador Dosamat - Dabi Atlante.
Dos resíduos de amálgama obtidos foram pesados , em balança de precisão MLW-Alemanha (Figura 6), 5 g. que foram divididos em 1 g. para cada tubo de ensaio utilizado.
FIGURA 6. Balança de precisão (MLW-Alemanha).
Os conjuntos, para cada líqüido testado, foram colocados em um suporte de madeira, sendo realizadas cinco repetições para cada substância química testada. O suporte de madeira contendo os conjuntos foi colocado em um recipiente fechado evitando assim a contaminação com o meio externo, Figura 7.
FIGURA 7. Recipiente fechado contendo os experimentos.
O tubo de ensaio contendo o papel de filtro impregnado com cloreto de paládio era examinado diariamente, sempre no mesmo horário, sendo que os resultados foram anotados (apêndice), até que a passagem do vapor de mercúrio pudesse ser detectada, marcando o papel de filtro com coloração preta, conforme pode ser visto na Figura 8.
FIGURA
8. Tubo
de ensaio, contendo papel de filtro previamente impregnado com cloreto
de paládio. A cor preta evidencia a presença de mercúrio.
PdCl2 + Hg0® HgCl2 + Pd0
A Figura 1 mostra com clareza a área onde essa reação química de cor escura ocorreu, e a onde não ocorreu, em virtude de não ter havido contato com o mercúrio. Na Figura 1A observa-se que, o vapor de mercúrio foi revelado pelo cloreto de paládio que transformou-se em cloreto de mercúrio (cor escura). No ponto 1B, observa-se que não houve o escurecimento do papel, a área não escurecida indica não haver contato com o vapor de mercúrio.
Este teste foi repetido várias vezes, sempre com os mesmos resultado, ou seja, o cloreto de paládio ao entrar em contato com o vapor de mercúrio é imediatamente revelado por meio da cor escura do papel, mostrando a identificação deste metal pela solução de cloreto de paládio.
TABELA
I. Número de dias transcorrido, para detecção
do vapor de mercúrio. Cinco experimentos para cada uma das substâncias
testadas.
| EDTA
pH 7,3 |
EDTA
pH 6,0 |
Álcool | Água | Fixador
Radiog. |
Propile-noglicol | Óleo
Vegetal |
Óleo
Mineral |
Revelador
Radiog. |
|
| Exp. 1 |
|
|
|
|
|
|
|
|
|
| Exp. 2 |
|
|
|
|
|
|
|
|
|
| Exp. 3 |
|
|
|
|
|
|
|
|
|
| Exp. 4 |
|
|
|
|
|
|
|
|
|
| Exp. 5 |
|
|
|
|
|
|
|
|
|
Os 45 dados amostrais (Tabela I) utilizados neste estudo foram os valores do número de dias transcorrido, para a detecção da passagem do vapor de mercúrio. Esse número total de dados resulta do produto fatorial de nove substâncias químicas (EDTA pH=7,3, EDTA pH=6,0, Álcool 96%, Água, Fixador Radiográfico - Kodak -, Propileno Glicol, Óleo Vegetal, Óleo Mineral e Revelador radiográfico - Kodak) por 5 repetições para cada uma das amostras testadas: 9 X 5 = 45.
Foram realizados testes preliminares, visando verificar se a distribuição dos dados amostrais seria normal, a fim de definir o tipo de estatística a ser utilizado (estatística paramétrica ou não paramétrica). Para isso, foi usado um programa de computador desenvolvido no Departamento de Estomatologia da Faculdade de Odontologia de Ribeirão Preto da Universidade de São Paulo, pelo Prof. Dr. Geraldo Maia Campos.
Comparou-se a distribuição amostral com uma distribuição de freqüência padrão, com intervalos de classe baseados na média e no desvio padrão da amostra, que são os pontos característicos da curva normal (Tabela II).
TABELA
II. Distribuição de freqüência: Valores originais.
| A. Freqüências por intervalos de classe: | |||||||||||||||||||
| Intervalos de classe: |
|
|
|
|
|
|
|
||||||||||||
| Freqüências absolutas: |
|
|
|
|
|
|
|
||||||||||||
| Em valores percentuais: |
|
|
|
|
|
|
|
||||||||||||
| B. Freqüências acumuladas: | |||||||||||||||||||
| Intervalos de classe: |
|
|
|
|
|
|
|
||||||||||||
| Freqüências absolutas: |
|
|
|
|
|
|
|
||||||||||||
| Em valores percentuais: |
|
|
|
|
|
|
|
||||||||||||
Uma vez calculadas as freqüências absolutas percentuais por intervalos de classe e acumuladas, foram traçadas duas curvas superpostas com base nos percentuais acumulados de freqüências, uma correspondente à curva normal matemática e a outra à distribuição amostral experimental. A discrepância entre as duas curvas demonstra seu grau de aderência. Pelo gráfico da Figura 9, observa-se não existir sobreposição das duas curvas, indicando a não normalidade da distribuição.
FIGURA 9. Traçado da curva normal matemática e da curva de distribuição amostral experimental. Observa-se que não ocorre sobreposição dos percentuais acumulados de freqüência referentes às curvas experimental e normal.
Para
elucidar ainda mais, realizou-se um teste de aderência
(pelo
X2) da curva experimental com a curva normal matemática (com a mesma
média e o mesmo desvio-padrão da curva experimental). Os
resultados estão expressos na Tabela III.
TABELA
III. Teste de aderência à curva normal: Valores originais.
| A. Freqüências por intervalos de classe: | |||||||||
| Intervalos de classe: |
|
|
|
|
|
|
|
||
| Curva normal: |
|
|
|
|
|
|
|
||
| Curva experimental: |
|
|
|
|
|
|
|
||
| B. Cálculo do Qui quadrado: |
|
||||||||
| Graus
de liberdade:
Valor de Qui quadrado: Probabilidade de Ho: |
4
20,13 0,05% |
|
|||||||
O resultado (x2= 20,13) para 4 graus de liberdade indica uma probalidade menor que 1% da curva testada ser normal.
Continuando, traçou-se o histograma de freqüências da amostra experimental e, ao mesmo tempo, sobrepôs-se a ele o traçado da curva normal matemática com a mesma média e o mesmo desvio-padrão da curva experimental, afim de servir como termo de comparação (Figura 10).
FIGURA 10. Histograma da distribuição de freqüências da amostra experimental, com sobreposição da curva normal matemática, ambas com a mesma média e o mesmo desvio-padrão. Note-se a ausência de correspondência entre as distribuições.
Os testes realizados levaram à conclusão de que a distribuição dos dados experimentais deste trabalho, referentes à emissão do vapor de mercúrio frente às substâncias testadas para armazenagem, não eram homogêneas e não tinham distribuição normal.
Diante
disso, a aplicação da análise estatística paramétrica
estava contra-indicada, optando-se portanto, pela análise estatística
não-paramétrica para dados independentes, selecionando-se
para isso o teste de Kruskal-Wallis, cujos resultados são mostrados
na Tabela IV.
TABELA
IV. Teste de KRUSKAL-WALLIS.
| Valor
de (H) de Kruskal-Wallis calculado:
Valor de c 2 para 8 graus de liberdade: Probabilidade de Ho para esse valor: |
43,7686
43,77 0,00 |
|
|
|
O teste de Kruskal-Wallis indicou que os resultados são significante diferentes ao nível de 1% de probabilidade para Ho.
A seguir, compararam-se as médias dos postos das amostras, e os resultados estão reunidos na Tabela V.
TABELA
V. Comparação entre as diferenças entre as médias
dos postos dos dados amostrais e sua interpretação estatística.
|
(comparações duas a duas) |
|
(a =0,001) |
|
||
| EDTA 7 | X | EDTA 6 |
12,5000
|
|
|
| EDTA 7 | X | Álcool |
0,0000
|
|
|
| EDTA 7 | X | Água |
22,5000
|
|
|
| EDTA 7 | X | Fixador |
27,5000
|
|
|
| EDTA 7 | X | Propileno |
7,5000
|
|
|
| EDTA 7 | X | O. Vegetal |
17,5000
|
|
|
| EDTA 7 | X | O. Mineral |
10,5000
|
|
|
| EDTA 7 | X | Revelador |
9,5000
|
|
|
| EDTA 6 | X | Álcool |
12,5000
|
|
|
| EDTA 6 | X | Água |
10,0000
|
|
|
| EDTA 6 | X | Fixador |
15,0000
|
|
|
| EDTA 6 | X | Propileno |
5,0000
|
|
|
| EDTA 6 | X | O. Vegetal |
5,0000
|
|
|
| EDTA 6 | X | O. Mineral |
23,0000
|
|
|
| EDTA 6 | X | Revelador |
22,0000
|
|
|
| Álcool | X | Água |
22,5000
|
|
|
| Álcool | X | Fixador |
27,5000
|
|
|
| Álcool | X | Propileno |
7,5000
|
|
|
| Álcool | X | O. Vegetal |
17,5000
|
|
|
| Álcool | X | O. Mineral |
10,5000
|
|
|
| Álcool | X | Revelador |
9,5000
|
|
|
| Água | X | Fixador |
5,0000
|
|
|
| Água | X | Propileno |
15,0000
|
|
|
| Água | X | O. Vegetal |
5,0000
|
|
|
| Água | X | O. Mineral |
33,0000
|
|
|
| Água | X | Revelador |
32,0000
|
|
|
| Fixador | X | Propileno |
20,0000
|
|
|
| Fixador | X | O. Vegetal |
10,0000
|
|
|
| Fixador | X | O. Mineral |
38,0000
|
|
|
| Fixador | X | Revelador |
37,0000
|
|
|
| Propileno | X | O. Vegetal |
10,0000
|
|
|
| Propileno | X | O. Mineral |
18,0000
|
|
|
| Propileno | X | Revelador |
17,0000
|
|
|
| O. Vegetal | X | O. Mineral |
28,0000
|
|
|
| O. Vegetal | X | Revelador |
27,0000
|
|
|
| O. Mineral | X | Revelador |
1,0000
|
|
|
| * Significância ao nível de 0,1% | |||||
Pela análise da Tabela V, observa-se que não há diferença estatística entre as substâncias testadas, EDTA 7 e Álcool, o mesmo ocorrendo entre o Óleo mineral e Revelador Radiográfico. Todavia, quando da comparação entre as outras substâncias, verificamos que existe significância entre as testadas.
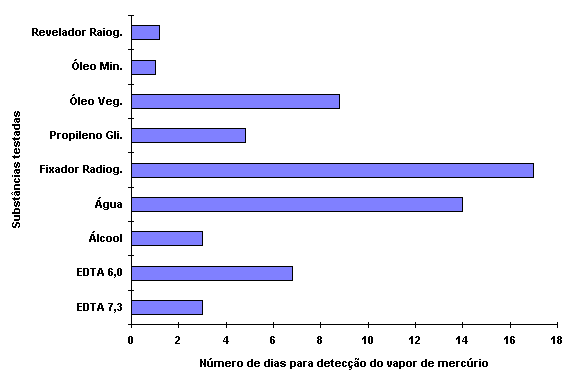
A
Figura 11 representa e evidencia melhor o tempo médio, transcorrido
para a detecção do vapor de mercúrio emitido pelos
resíduos de amálgama, em diferentes substâncias para
armazenagem. Mostrando que, em média, o Fixador radiográfico
impede a passagem do vapor de mercúrio por 17 dias , a Água
por 14 dias, o Óleo Vegetal por 8,8 dias, o EDTA pH 6,0 por 6,8
dias, o Propileno Glicol por 4,8 dias, o EDTA pH 7,3 e o Álcool
por 3 dias, o Revelador radiográfico por 1,2 dias e o Óleo
mineral por 1,2 dias.
 |
FIGURA 11. Tempo médio, transcorrido para detecção do vapor de mercúrio.
O amálgama dental é um dos materiais restauradores mais usados na clínica odontológica. Um dos seus componentes é o mercúrio, cujo uso tem sofrido algumas restrições em diferentes períodos, apesar das restaurações de amálgama terem prestado excelentes serviços por mais de 150 anos.
Nos consultórios odontológicos, o risco de contaminação é bem elevado, já que as fontes de mercúrio são muitas, níveis elevados de vapores de mercúrio foram encontrados em consultórios odontológicos por JOSELOW (1968).
Diversos autores como TEIXEIRA et al (1970), CHAN & SVARE (1972), WILSON & WILSON (1982) entre outros estudaram a emissão de vapores de mercúrio em restaurações de amálgama. Sendo que os resultados, foram unânimes em apresentar elevada evaporação de mercúrio proveniente das restaurações. MAREK (1984) em minucioso estudo verificou que durante a mastigação há evaporação de mercúrio.
A intoxicação do cirurgião-dentista e da auxiliar dá-se pela pele ou pela inalação de vapores. Sabe-se que a volatilização do mercúrio aumenta com o aumento da temperatura ambiente. Se a temperatura se eleva de 20oC para 50oC, ocorre um aumento de oito vezes na volatilização, RUPP & PAFFENBARGER (1971).
Por outro lado, são sabidos os danos ocasionados por estes vapores de mercúrio, sinais não específicos da exposição têm sido chamados de Síndrome Astênica Vegetativa, incluindo sinais e sintomas como fadiga, anorexia, perda de peso e distúrbios gastrointestinal, conforme relato de LANGHAN (1987). Autores como VANDENBERGE et al (1977), GOODMAN & GILLMANS (1980), NALEWAY et al (1985) e WAEFVINGE (1995), reafirmaram estes danos à saúde dos cirurgiões-dentistas.
Muitas fontes potenciais de contaminação que podem elevar o mercúrio a níveis muito perigosos existem no consultório odontológico: derramamento acidental, higiene inadequada do ambiente de trabalho, excesso de mercúrio de amálgama recém-preparado, amalgamadores mecânicos, condensadores ultra-sônicos, aquecimento de porta-amálgama para desalojar partículas presas, falhas na refrigeração durante a remoção de restaurações antigas, esterilização imprópria de instrumentos contaminados com mercúrio, vazamento nos dispensadores, estocagem inadequada de restos de amálgama, esgotos, lixos e tapetes.
O derramamento de mercúrio e subsequente acúmulo no carpete ou nas frestas dos pisos constituem uma das maiores fontes de contaminação. LANGHAN (1987) encontrou pouca diferença entre as concentrações de vapores de mercúrio no ar de consultórios odontológicos com carpete ou piso liso, isso porque cada piso oferece um problema quanto a limpeza. O mercúrio em pisos comuns tende a se espalhar, dificultando a limpeza, já no carpete, o mercúrio fica contido em uma pequena área, porém, sua limpeza é difícil. Quando o mercúrio é derramado, dispersa-se em pequenas porções e aumenta sua tendência à evaporação.
A estocagem dos resíduos de amálgama é, entre tantas, uma potencial fonte produtora de vapor de mercúrio. Na literatura não há consenso de como o amálgama deve ser armazenado no consultório. MAGRO et al (1994), afirmaram que "todo resto de amálgama deve ser armazenado em recipiente fechado, sob solução fixadora radiográfica" o que pode ser confirmado pelos resultados da presente pesquisa. Uma vez que o fixador radiográfico impediu a passagem do vapor de mercúrio por dezessete dias, sendo das substâncias testadas a que melhor resultados apresentou. Das substâncias testadas, o óleo mineral e o revelador radiográfico foram as que ofereceram menor resistência a passagem do vapor de mercúrio.
Os resultados do presente trabalho são coincidentes com os de BOYER & CHAN (1977) e EMLER & CARDONA (1985) deixando claro a existência concreta da evaporação de mercúrio nos resíduos de amálgama. Os resultados obtidos são razões mais do que suficientes para alertar os cirurgiões dentistas quanto a importância de prevenir a contaminação do meio ambiente e do consultório pelo mercúrio. Outro fator fundamental é a importância que deve ser dada ao tratamento dos resíduos de amálgama após os dezessete dias de armazenamento, uma vez que ao lançar os resíduos de amálgama na rede de esgoto estará expondo todo o meio ambiente aos efeitos deletérios do mercúrio.
A prevenção da exposição ambiental ao mercúrio pode ser razoavelmente conseguida pelos níveis de mercúrio no ambiente e a observância a certos limites propostos. Estes limites se basearam nas concentrações de mercúrio já registradas em distintas partes do mundo e nas quais não se detectaram efeitos nocivos sobre a saúde da população exposta. O presente trabalho mostra que a evaporação de mercúrio em resíduos de amálgama, pode contaminar o meio ambiente, uma vez que, em água a evaporação mostrou-se presente em quatorze dias. Reforçando a tese de que, o cirurgião-dentista não deve descartar os resíduos de amálgama direto na rede de esgoto, pois estará contaminando todo o ecossistema.
Para avaliação e controle da contaminação ambiental, são empregados organismos vivos dos ecossistemas que denunciam precocemente a presença do mercúrio (bioindicadores), seja porque são concentradores do metal, seja porque mais cedo manifestam seus efeitos tóxicos, pode ser de grande valia no sentido de que, funcionam como sentinelas avançadas, informando sobre a evolução da poluição. Os resíduos de amálgama provenientes do consultório odontológico podem contaminar o meio ambiente, trazendo sérios perigos para a população, como os evidenciados por LINDBERG et al. (1987).
Quanto à despoluição, nos últimos tempos tem-se dedicado esforços de pesquisa científica e tecnológica no sentido de se criar e controlar processos para remoção da carga poluidora de mercúrio, principalmente de corpos hídricos. Na presente pesquisa, fica claro que o cirurgião-dentista deverá fazer um controle rígido dos resíduos de amálgama provenientes das restaurações, auxiliando assim a não poluição do meio ambiente, evitando também sanções de ordem legais. Segundo a Legislação brasileira, Portaria 3214 do Ministério do Trabalho, o nível de exposição máxima, considerado seguro para exposição ocupacional, é de 0,05 microgramas de vapor de mercúrio por metro cúbico de ar.
Existem hoje instrumentos legais que visam minimizar a contaminação ambiental. No Brasil, recentemente, o Governo Federal, denunciando a pressão crescente exercida pôr vários segmentos da sociedade preocupados com a preservação dos recursos naturais e manutenção da qualidade da vida, tem adotado uma série de medidas legais objetivando controlar o uso e os riscos do uso do mercúrio em todas as atividades. Portanto caso o cirurgião-dentista não proceda o correto tratamento dos resíduos de amálgama estará infringindo a Portaria no 3214 do Ministério do Trabalho.
No consultório odontológico, o controle a exposição ocupacional a esse metal, nas mais diferentes formas em que ele ou seus compostos são empregados, pode e deve ser feito pela apuração de algumas medidas técnicas que devem ser salientadas.
Entre as mais importantes medidas técnicas a prevenção da exposição ocupacional ao mercúrio temos: 1o- avaliação permanente da presença de vapores de mercúrio no ambiente do consultório odontológico, podendo ser usado para este teste, o mesmo utilizado no presente trabalho, ou seja, papel de filtro com cloreto de paládio exposto no ambiente do consultório para detecção de vapores de mercúrio; 2o- armazenamento do mercúrio em recipientes fechados e inquebráveis, sendo que a tampa deste recipiente deve ser envolvida com papel de filtro embebido em cloreto de paládio, pois qualquer vazamento poderá ser detectado; 3o- uso somente de cápsulas que permaneçam seladas durante a amalgamação e mesmo assim a colocação de papel de filtro com cloreto de paládio é indicado; 4o- armazenamento dos resíduos de amálgama em recipientes fechados contendo solução fixadora radiográfica, nunca por um período maior que dezessete dias, de acordo com os resultados obtidos no presente trabalho.
Decorridos o período de segurança, todos os resíduos de amálgama deveriam ser enviados a Centros de reciclagem para que o mercúrio e os elementos componentes do amálgama fossem reciclados e reaproveitados. Estes Centros de reciclagem irão evitar a contaminação do cirurgião-dentista e do meio ambiente.
Porém, quando o cirurgião-dentista não encaminhar para os Centros de reciclagem, os resíduos de amálgama, deve após o décimo sétimo dia de armazenamento tratar estes resíduos em solução de enxofre para só depois disto lança-lo ao meio ambiente.
Outro fator importante a ser considerado é o nível de vapor de mercúrio no ambiente dos consultórios odontológicos. Segundo MANTYLA & WRIGHT (1976), nos Estados Unidos, pelo menos 10% dos consultórios odontológicos apresentaram níveis de vapor de mercúrio no ar mais elevados que o limite máximo permitido.
Sem
dúvida nenhuma, o método proposto abre a possibilidade prática
do próprio cirurgião-dentista detectar o vapor de mercúrio
no ambiente do consultório, de maneira simples, prática e
barata. Basta para tanto, que o cirurgião-dentista prepare uma solução
de cloreto de paládio a 1% e umedeça papel de filtro Watman
com tal solução. Após a secagem do papel em ambiente
isento de mercúrio, colocará este papel impregnado com cloreto
de paládio no ambiente do consultório. Como ficou demonstrado
na presente pesquisa, quando o papel de filtro impregnado com cloreto de
paládio entrar em contato com o vapor de mercúrio irá
escurecer, mostrando ao cirurgião-dentista a presença do
mercúrio no seu ambiente de trabalho.
Com base na metodologia empregada e nos resultados obtidos, parece lícito concluir que:
1. A solução de cloreto de paládio revela a presença de vapor de mercúrio nas condições do presente trabalho.
2. Nenhuma das soluções utilizadas foram eficientes no bloqueio da passagem do vapor de mercúrio.
3. A solução de EDTA e Álcool 96 GL foram as de menor eficiência, pois impediram a passagem de vapor de mercúrio por apenas três dias.
4.
A solução de Fixador Radiográfico (Kodak) foi aquela
que se mostrou mais eficiente, pois impediu a passagem de vapor de mercúrio
por dezessete dias.
Fez-se a identificação qualitativa do vapor de mercúrio captado de resíduos de amálgama de prata, em diversos meios de armazenagem, com o uso do cloreto de paládio.
Os resíduos de amálgama foram armazenados em: solução de EDTA pH 7,3, solução de EDTA pH 6,0, álcool 96%, água, fixador radiográfico, propilenoglicol, óleo vegetal (soja), óleo mineral e revelador radiográfico.
Os
resultados permitiram concluir que: a solução de cloreto
de paládio revela a presença de vapor de mercúrio
nas condições do presente trabalho. Nenhuma das soluções
utilizadas foram eficientes no bloqueio da passagem do vapor de mercúrio.
A solução de EDTA e Álcool 96%, foram as de menor
eficiência, pois impediram a passagem de vapor de mercúrio
por apenas três dias. A solução de Fixador Radiográfico
(Kodak) foi aquela que se mostrou mais eficiente de todas as testadas,
pois impediu a passagem de vapor de mercúrio por dezessete dias.
A qualitative identification of mercury vapor taken up by silver amalgam residues was performed in several storage media using palladium chloride.
The amalgam residues were stored in EDTA solution, pH 7.3, EDTA solution, pH 6.0, 96% alcohol, water, radiographic fixative, propyleneglycol, vegetable oil, (soy), mineral oil and radiographic developer.
The results led us conclude that the palladium chloride solution revealed the presence of mercury vapor under the conditions of the present study. Name of the solutions studied were efficient in blocking the passage of mercury vapor. The EDTA solution and 96% alcohol were the least efficient since they prevented the passage of mercury vapor only for three days. The radiographic fixative solution (Kodak) was the most effective of all tested media since it prevented the passage of mercury vapor for 17 days.
AMERICAN DENTAL ASSOCIATION - Council on dental materials and devices. Mercury surverys in dental offices. J. Amer. dent. Ass., v. 89, n. 4, p. 900-1, 1974.
ANCONA, A.; RAMOS, M.; SUAREZ, R. & MACOTELA, E. Mercury sensitivity in a dentist. Contact dermatitis, v. 8, p. 218, 1982.
ANDERSON, M.H. Mercury leakage during amalgam trituration. Oper. Dent., v. 13, p. 185-90, 1988.
BAUER, J.G. & FIRST, H.A. The toxicity of mercury in dental amalgam. J. Calif. Dent. Assoc., v. 10, p. 47-61, 1982.
BERGENHOLTZ, A. Mutiple Polypous of the Oral Mucosa With Regression After Removal of Amalgam Fillings. Acta Odontologica Scandinavica, v. 23, p. 111-23, 1965.
BJORKMAN, L. & LIND, B. Factors influencing mercury evaporation rate from dental amalgam fillings. Scand. J. Dent. Res., v. 100, n. 6, p. 354-60, 1992.
BJORKMAN, L.; PALM, B.; NYLANDER, M.; NORDBERG,M. Mercury and selenium distribution in human kidney cortex. Biol. Trace. Elem. Res., v.40, n. 3, p. 255-65, 1994.
BLACK, G.V. in ZIFF S. Amálgama a toxica bomba relógio. Editora Vega Lux Ltda, 1a. ed., 1987.
BLOCH, P. & SHAPIRO, J.M. Summary of the international practice. J. Amer. dent. Ass., v. 104, p. 489-90, 1982.
BOYER, D.B. & CHAN, K.C. The effect of burnishing on the mercury vapor emission of amalgam. J. dent. Res., v. 56, p. 1330, 1977.
BRASIL, Ministério do Trabalho. Portaria No 3214. Diário Oficial da União, 08/06/1978. NR-7, alterada pela Portaria 12. Secretaria de Segurança e Medicina do Trabalho, Ministério do Trabalho.
BRUN, R. Epidemiology of contact dermatitis in geneva (1000 casos). Contact Dermatitis, v. 1, p. 214-217, 1975.
BUCHWALD, H. Exposure of dental workers to mercury. Am. Ind. Hyg. Ass. J., v. 33, p. 492-502, 1972.
CHAN, K.C. & SVARE, C.W. Mercury vapor emission from dental amalgam. J. dent. Res., v.51, p. 555-59, 1972.
CHEEK, D.B. The Effect of Mercurous Chloride (Calomel) and Epinephrine (Sympathetic Stimulation) on Rats The Importance of the Findigs to Mechanisns in Infantile Acrodynia Pediatrics. v. 23, p. 302, 1959.
COOK, T.A.; YATES, P.O. Fatal mercury intoxication in a dental surgery assistant. Brit. dent. J., v. 127, n. 11, p. 553-555, 1969.
CRAWCOUR, D.K. The Story of Dentistry. 3a. ed., Dental Items of Interest Publishing, New York, 1833.
DAHHAN, S.S. & ORFALY, H. Electrocardiographic Changes in Mercury Poisoning. American Journal of Cardiology, v. 14, p. 178-183, 1964.
DJERASSI, E. & BEROVA, W. The possibilitieis of allergic reaction from silver amalgam restorations. International Dental Journal, v.4, n. 4, p. 481-88, 1969.
ELIZAUR BENITEZ, A.B.C.; FULLER, J.B.; SALGADO, P.E.; GABRIELLI, F.; DINELLI, W. & GABRIELLI, A.P.R. Amálgama dental: estudo in vitro da liberação de mercúrio, através de espectrofotometria de absorção atômica, em função do tipo de ligas, polimento e tempo. Rev. Odontol. Univ. São Paulo, v. 9, n. 1, p. 39-43, jan./mar. 1995.
EMLER, B.F. & CARDONE, M.S. An Assessment of mercury in mouth air. Journal of Dental Research, v. 65, p. 311, 1985.
FEIGL, F.; ANGER, V. Spot tests in inorganic analysis. 6a ed. Amsterdan, Elsevier Publishing Company, 1972, 305 p.
FINNE, K. Oral lichen planus and contact allergy to mercury. International Journal of Oral Surgery, v. 11, p. 236-239, 1982.
FLAGG, J.F. The Choice of Proper Filling Material. Acta odontologica Scandinavica, v. 22, n. 22, p.355-58, 1870.
FREDEN, H. Mercury Content in Gengival Tissues Adjancent to Amalgan Filling. Odontologica Review, v. 25, n. 2, p. 207-210, 1974.
FRIBERG, K. Kidney Injury After Chronic Exposure to Inorganic Mercury. Archives of Industrial Hygiene and Occupational Medicine, v. 8, p. 149-53, 1953.
FRYKHOLM, K.O. On Mercury From Dental Amalgam Its Toxic and Allergic Effects and Some Comments on Occupational Hygiene. Acta Odontologica Scandinavica, v. 15, p. 1-108, 1957.
GERSTNER, H.B. & HUFF, J.E. Clinical Toxicology of Mercury. Journal of Toxicology and Environmetal Health, v. 2, n. 3, p. 491-526, 1977.
GETTLEMAN, L. What can we do about the mercurophobes. Oper. Dent., 11:78-80, 1986.
GOLDMAN, M. & BLACKBURN, P. The Effect of Mercury Chloride on Thyroid Function in the Rat. Toxicology and Applied Pharmecology, v. 48, p. 49-55, 1979.
GOODMAN k. & GILLMANS, H. The Pharmacological Basis of Therapeutics. 6a. ed, Macmillan Publishing, 1980, 563p.
GOYER, R.A. Toxic effects of metals. In: KLAASEN, C.D.; AMDUR, M.O.; DOULL, J. Casarett and Daulls toxicology the basic science of poisons. 3a edição, Macnillan, New York, 1986, 605 p.
GRONKA, P.A.; BOBKOSKIE, R.L.; TOMCHICK, G.J.; BACH, F. & RAKOW, A.B. Mercury vapor exposures in dental offices. J. Amer. dent. Ass. v. 81, n. 4, p. 923-925, 1970.
GROSSMAN, L.I. & DANNENBERG, J.R. Amout of mercury vapor in air of dental offices and laboratories. J. dent. Res. 28:435-8, 1949.
HAHN, L.J.; KLOIBER, R.; VIMY, M.J. Dental "silver" tooth fillings: asource of mercury exposure reveled by whole-body image sean and tissue analyssis. Faseb Journal, v. 3, n. 14, p. 2641-2646, 1989.
HARRIS, C.A. History of mercury and mercurialism. State Journal of Medicine, v. 81, p. 1902-1909, 1840.
HARRIS, D. The dental working enviroment and risk of mercury exposure. J. Am. dent. Ass., v. 97, p. 811-815, 1978.
HAY W.J.; RICHARDS, A.G.; McMENEMEY, W.H. & CUMINGS, J.N. Organic Mercurial Encephalopathy. Journal of Neurology and Neurosurgical Psychiatry, v. 26, p. 199-202, 1963.
HOLLAND, R.I. Release of mercury vapor from corroding amalgam in vitro. Dental Materiais, v. 9, p. 99-103, 1993.
HUNTER, M. Posisoning by Methylmercury Compounds. Quaterly Journal of Medicine, v. 33, p. 193-206, 1940.
HURSH, J.B.; CLARKSON, T.W.; NOWAK, T.V.; PABICO, R.C.; McKENNA, B.A., MILLES, E. & GIBB, F.R. Prediction of kidney mercury content byisotope techniques. Kidney International, v. 27, n. 6, p. 898-907, 1985.
JOSELOW, M.M. Absortion and excretion of mercury in man. Arch Environment Hilth, v. 17, n. 2, p. 39-43, 1968.
KATSUKI, M. On the Disease of Central Nervous System in Minemata District With Unknown Etiology With Special References To Clinical Observations. Kumamoto Igakki Zasshi, v. 31, p. 110-121, 1957.
KELMAN, G.R. Notes and miscellanea: Urinary mercury excretion in dental personnel. Bristish Journal of Industrial Medicine, London, v. 35, n. 3, p. 262-65, 1978.
LANGHAN, D.C. The use of mercury in dentistry: a critical review of the recente literature. J. Am. Dent. Assoc. v. 115, n. 6, p. 867-880, 1987.
LARINI, L. & SALGADO, P.E.T. Exposição de cirurgiões dentistas ao mercúrio. Rev. Cienc. farm. São Paulo, v. 3, p. 41-46, 1981.
LINDBERG, S.; STOKES, P.; GOLDBERG, E.; WREN, C. Group report: Mercury. In: HUTCHINSON, T.W.; MEEMA, K.M. ed. Lead, mercury, cadmium and arsenic in the environment. Chichester, Brisbane, John Wiley & Sons, p. 17-34, 1987.
LIPPMANN, D.S. Mercurial poisoning and sensitivity from cooper and silver amalgam fillings. Quintescenz, v.12, p. 53-54, 1962.
MACKERT JR., J.R. Lymphocyte levels in subjects with and without amalgam restorations. J. Am. Dent. Assoc., v. 12, n. 2, p. 49-53, 1991.
MAGOS, L. Neurotoxicity, anorexia and the preferential choice of antidote in methylmercury intoxicated rats. Neurobehavioral Toxicological Teratology, v.4, p. 643-46, 1967.
MAGRO, A.C.; BASTOS, P.A.M. & NAVARRO, M.F.L. Segurança no uso do mercúrio em restaurações de amálgama. Rev. Odontol. Univ. São Paulo, v. 8, n. 1, p. 1-6, jan./mar. 1994.
MANDEL, I.D. Amalgam hazards: an assessment of research. J. Am. Dent. Assoc., v. 122, n.6, p. 62-65, 1991.
MANDETTA, S. Brunidura da superfície do corpo de prova, de amálgama após a escultura; contribuição para o estudo da influência sobre o conteúdo de mercúrio. São Paulo, 1972./ Tese - Doutoramento - Faculdade de Odontologia de São Paulo - U.S.P.
MANTYLA, D.G. & WRIGHT, O.D. Mercury toxicity in the dental office: as neglecter problem. J. Am. Dent. Assoc., v. 92, p. 1189-1194, 1976.
MAREK, M. Acceleration of corrosion of dental amalgam by abrasion. Journal of Dental Research, v. 63, n. 7, p. 1010-1013, 1984.
MILLER, E.G. Prevalence of mercury hipersensitivity in dental students. Journal of Dental Research, v. 64, p. 338, 1985.
MOBACKEN, L. Oral lichen planus: Hipersensitivity to dental restoration material. Contact Dermatitis, v. 10, n. 1, p. 11-15, 1984.
NALEWAY, C.; SAKAGUCHI, R. & MITCHELL, E. Urinary mercury levels in US dentists, 1975-1983: Review of Health Assessment Program. J. Am. Dent. Assoc., v. 111, n.1, p. 37-42, 1983.
NASCIMENTO, T.N.; RIBEIRO, S.A.; CENTOLA, A.L.B.; CAMPOS, S.M. Fuga de mercúrio ocorrida durante a trituração mecânica da amálgama. Ver. Portuguesa de Odontologia, v.15, p.9-14, 1991.
NEBENFUHRER, L. Mercury allergy in Budapest. Contact Dermatitis, v. 10, n. 2, p. 121-22, 1983.
NILNER, K. Effect of dental amalgam restorations on the mercury content of nerve tissues. Acta Odontol. Scand. 43:303-7, 1985.
NILSSON, B. & NILSSON, B. Mercury in dental practice. The working enviroment of dental personnel and their expossure to mercury vapor. Swed. dent. J., 10:1-14, 1986.
POPESCU, H.I. Chromosome Aberration Induced by Occupational Exposure to Mercury. Archives of Environmental Health, v. 34, p. 461-463, 1979.
REUHL, K.R. & CHANG, L.W. Neurotoxicology, v. 1, p. 21-55, 1979.
RICHARDS, J.M. & WARNER, P.J. Mercury vapor released durint the removal of old amalgam restorations. Brist. dent. J., v. 159, p. 231-232, 1985.
ROTHSTEIN, A. & HAYES, A.D. Journal of Pahrmacology and Experimental Therapy, v. 130, p. 166-76, 1960.
ROTHSTEIN, A. Mercaptans. The Biological Targets for Mercurials. In: MILLER, M.W. & CLARKSON, T.W. Mercury, Mercurials. Charles Editores, Springfield, Ilinois, 1971, 326 p.
RUPP, N.W. & PAFFENBARGER, G.C. Significance to health of mercury used in dental practive: a review. J. Amer. dent. Ass. 82:1401-7, 1971.
SALGADO, P.E. Risco ocupacional ao mercúrio na Odontologia. RGO, v. 35, n. 11, p. 183-7, 1987.
SAQUY, P.C. & PÉCORA, J.D. A Ergonomia e as Doenças Ocupacionais do Cirurgião-Dentista. Manual Dabi Atlante, 1994, 31 p.
SAQUY, P.C. & PÉCORA, J.D. Orientação Profissional em Odontologia. Editora Santos, 1a. edição, São Paulo, 1996. 67p.
SHARHISTAM, H.; SHIHAB, K. & HADDAD, I.K. Mercury in hair as an indicator of total body burden. In: Who. World Health Organization Conference on Intoxication due to Alkylmercury. Treated Seed. Baghdad, 1974. Geneve: WHO, p. 105-112, 1976.
SILVA FILHO, F.P.M. & GANDINI JUNIOR, L.G. Os perigos do mercúrio no consultório dentário. Rev. Ass. paul. Cirug. Dent. v. 32, n. 5, 1978.
SNYDER, R.D. The Involuntary Movementes of Chronic Mercury Poisoning. Archives of Neurology, v. 26, p. 379-81, 1972.
STEINWALL, O. & SNYDER, H. Brain Uptake of C14 - Cyclo-Leucine After Damage To Blood-Brain Barrier by Mercuic Ions. Acta Neurologica Scandinavica, v. 45, p. 369-75, 1969.
STOCK, A. The Effect of Two Organic Mercury Compounds on Human Leukocytes In Vitro. Naturwissenschaften, v. 23, p. 453-56, 1935.
STOCK, A. The Hazards of Mercury Vapor. Zeitsch Angew Chem., v. 39, p. 461-88, 1926.
STOZ, F.; AICHAM, P.; JOVANOVIC, S.; STEUER, W. & MAYER, R. Effects of new dental amalgam filling in pregnancy on Hg concentration in mother and child. Whit consideration for possible interactions between amalgam and precious metals. Zentralbl Gynakol, v.117, n. 1, p. 45-50, 1995.
STOZ, F.; AICHAM, P.; JOVANOVIC, S.; STEUER, W. & MAYER, R. Is a generalized amalgam ban justified? Studies of mothers and their newborn infants. Geburtshile Perinatol, v. 199, n. 1, p. 35-41, 1995.
SURMONT, P.; ENODY, E. Evaluation of amalgam sepators. Rev. Belge. Med. Dent., v. 48, n. 4, p. 17-26, 1993.
TAVEAU, M. History of dental and oral science in America, prepared under direction of the American Academy of Dental Science. Philadelphia, pennsylvania, 1826.
TEIXEIRA, L.C.; KAMMERMERYER, K. & JOHNSON, W.W. Printing of mercury distribution on the surface of dental amalgams. J. Am. Dent. Assoc., v.81, p. 1159-62, 1970.
TILL, T. & MALY, K. Zum Nachweis Der Lyse Von Hg Aus Silber-Amalgam Von Zahnfullungen. Der Praktesche Arzt, v. 32, p. 1042, 1978.
VALE, S.A.L. Estudos Morfológico, Morfométrico e Estereológico das Alterações Presentes na Mucosa da Língua do Feto de Rato. Determinado pelo Mercúrio. Ribeirão Preto, 1993./ Tese - Doutoramento - Faculdade de Odontologia de Ribeirão Preto - U.S.P.
VANDEBERGE, J.; MOODIE, A.S. & KELLER, R.E. Blood serum mercury test report. J. Amer. Dent. Ass., v. 94, n. 6, p. 1155-7, 1977.
VIMY, M.J. & LORSCHEIDER, F.L. Intra-oral air mercury released from dental amalgam. Journal of Dental research, v. 64, p. 1069-1071, 1985.
VIMY, M.J.; TAKAHASHI, Y.; LORSCHEIDER, F.L. Material-fetal distribution of mercury (203 Hg) released from dental amalgam fillings. American Journal of Physiology, v.258, n. 4, p. 939-45, 1990.
WANNAG, A. & SKJAERASEN, J. Mercury accumulation in placenta and fetal membranes. A study of dental workers and their babies. Eviron Physiol Biochen, v. 5, n. 5, p. 348-52, 1975.
WARFVINGE, K. Mercury exposure of a female dentist before pregnancy. Br. Dent. Journal, v. 178, n. 4, p. 149-52, 1995.
WHITTE, R.R. & BRANT, R.L. Development of Mercury Hypersensitivity Among Dental Students. J. Am. Dent. Assoc. v. 92, p. 1204-07, 1976.
WILSON, S.J. & WILSON, H.J. Mercury leakage from disposable capsules. Brist. Dent. J., v. 17, n.7, p. 144-53, 1982.
YOSHINO, Y,; MOZAI, T. & NAKAO, K. Accumulation and Retentions of Mercury in the Mouse. Journal of Neurochemistry, v. 13, p. 1223-30, 1966.
ZIFF,
S. Silver dental fillings: the toxic time bomb. São Paulo,
Vega Luz, 1987.