Faculdades de Odontologia da UERJ e Faculdade de Odontologia de Ribeirão Preto - USP
Dissertação
de Mestrado
Ação dos géis clareadores que contêm peróxido de carbamida sobre a microdureza do esmalte humano
Bleaching gel agents actions with carbamide peroxide on human enamel microhardness
Co- Orientador : Prof. Dr. Jesus Djalma Pécora FORP - USP
Este
trabalho foi realizado no Laboratório de Pesquisa em Endodontia
do Departamento de Odontologia Restauradora da Faculdade de Odontologia
de Ribeirão Preto - USP
Rio
de Janeiro e Ribeirão Preto 1996
Rio
de Janeiro, 1996, 103p.
A Odontologia, como ciência e profissão, teve sua origem e desenvolvimento direcionados para a resolução de três problemas básicos: remoção da odontalgia, recuperação morfo-funcional dos dentes e restabelecimento da estética dental.
Historicamente, avaliando-se o componente estético dos dentes, observa-se que a característica cromática sempre foi um de seus atributos fundamentais, existindo registros de procedimentos que visavam deixar os dentes mais claros que datam de mais que 2000 anos (DALE, 1993).
No mundo moderno, com o conceito de estética cada vez mais valorizado, os dentes constituem um dos principais fatores na composição da integridade física e psicossocial do indivíduo. Um sorriso mostrando dentes saudáveis realça a expressão facial e indica auto-valorização.
Assim, a função dos dentes ultrapassa a atividade mastigatória e o indivíduo, principalmente aquele que exerce atividade profissional ligada diretamente ao público, passa a querer algo mais que elementos dentais íntegros, bem posicionados ou bem restaurados. Ele persegue o modelo de beleza estabelecido pelos padrões culturais da sociedade em que vive.
A alteração da cor natural dos dentes pode se dar devido fatores exógenos, endógenos, medicamentosos, iatrogênicos e ainda por trauma com ruptura de vasos sangüíneos da polpa coronária (DALE, 1993; JORDAN et al, 1994).
As descolorações exógenas são muito freqüentes e geralmente são resultado da deposição ou elaboração de substâncias cromáticas sobre a superfície dos dentes. As mais características são as causadas por alguns alimentos ou bebidas, por nicotina, por amálgama e por bactérias cromogênicas. A cor adquirida depende do agente causador. Normalmente essas alterações cromáticas são de fácil remoção, bastando uma profilaxia dental.
As alterações cromáticas endógenas são difíceis de serem tratadas, uma vez que o agente causal está incorporado à estrutura dentária, envolvendo esmalte e/ou dentina. São causadas por certas doenças, tais como: icterícia (amarelo - marrom), porfíria (púrpura), eritroblastose fetal (cinza). Defeitos de calcificação ou de desenvolvimento dental também promovem alterações cromáticas endógenas e, entre elas, pode-se citar: hipoplasia de esmalte (marrom), amelogênese imperfeita (amarelo - marrom), hipocalcificação do esmalte (branco) e dentinogênese imperfeita (cinza - marrom).
Entre as alterações causadas por medicamentos, pode-se citar as oriundas da ingestão excessiva de flúor (branco - amarelo - cinza - marrom), de tetraciclina (amarelo - cinza escuro) e de ferro (preto).
As alterações iatrogênicas podem ocorrer em virtude de procedimentos restauradores e/ou endodônticos incorretos ou descuidados.
Em dentes tratados endodonticamente, a perda da translucidez natural é decorrente da desidratação da estrutura dentinária coronária. Entretanto, alterações cromáticas podem ser causadas por descuido profissional em virtude da falta de uso de agentes irrigantes que promovam óxido-redução ou da permanência no interior da câmara pulpar de resíduos teciduais ou de materiais obturadores (pastas, cimentos e cones).
Após análise cuidadosa da etiologia e intensidade da alteração cromática, uma das opções de tratamento é o clareamento dental, por apresentar resultados estéticos bastante significativos, ser uma técnica conservadora e econômica, que pode ser realizada tanto em dentes vitais quanto em dentes desvitalizados após o tratamento endodôntico.
É essencial, portanto, que o profissional estabeleça um bom diagnóstico, já que só após a determinação da etiologia da alteração cromática é que se poderá propor o tratamento adequado e se terá um prognóstico para o caso.
Desde a segunda metade do século passado, observa-se que os cirurgiões-dentistas preocupam-se com o clareamento dental em dentes desvitalizados. Inúmeras tentativas foram realizadas e, em 1872, foi promovido um encontro científico na cidade de Berlim, cujo objetivo foi estudar o clareamento dental. Nessa oportunidade, BOGUE apresentou o ácido oxálico como agente clareador de dentes escurecidos pelo extravasamento de sangue no interior dos canalículos dentinários.
Muitos outros profissionais dedicaram-se à busca de soluções químicas capazes de clarear dentes escurecidos. Esses cirurgiões-dentistas eram bons conhecedores de química e propuseram potentes agentes oxidantes para promover o clareamento dental. Entre eles, podemos citar: WOODNUTT (1860) e TRUMAN (1881), Licor de Labarraque; MQUILLEN (1867), hipoclorito de cálcio; HARLAN (1884), cloreto de alumínio + peróxido de hidrogênio a 3%; KIRK (1893), dióxido de sódio; ABBOT (1918), peróxido de hidrogênio a 30%; PRINZ (1924), perborato de sódio; SALVAS (1938) perborato de sódio e água; NUTTING & POE (1963), perborato de sódio com peróxido de hidrogênio 30% e calor.
Em 1937, AMES preconizou a técnica de clareamento de dentes vitais em que usava, sobre a estrutura de esmalte, o peróxido de hidrogênio a 30% misturado com éter e aplicava o agente físico calor. De certa forma e com algumas modificações, essa técnica ainda tem adeptos nos dias atuais (SWIFT, 1988; AUN & MOURA, 1988; RADETIC, 1988; PAULA EDUARDO & AUN, 1993).
Um novo conceito de técnica de clareamento dental para dentes vitais que está muito difundido atualmente é o emprego do peróxido de carbamida a 10% (peróxido de uréia), que pode ser auto-administrado pelo paciente sob supervisão do cirurgião-dentista. Esse novo conceito foi proposto por HAYWOOD & HEYMANN (1989), e sofreu várias modificações com o decorrer do tempo no que diz respeito à concentração utilizada.
Qualquer que seja a substância clareadora empregada, o mecanismo de ação consiste na liberação de oxigênio nascente que, ao penetrar na estrutura dentária, ocasiona uma reação de óxido-redução com o corante, alterando quimicamente a sua estrutura, dando compostos de coloração clara.
O clareamento dental intracoronário realizado em dentes tratados endodonticamente tem sido considerado como um procedimento eficiente. Entretanto, evidências recentes sugerem que esse procedimento pode resultar em complicações significantes.
As reabsorções cervicais das raízes têm sido atribuídas à natureza tóxica do peróxido de hidrogênio, que pode penetrar através dos canalículos dentinários e atingir os tecidos periodontais (HARRINGTON & NATKIN, 1979; FRIEDMAN et al, 1988; PÉCORA et al, 1991; DAHLSTRON, 1993). além disso, LADO et al (1983) mostraram que o peróxido de hidrogênio a 30% desnatura a dentina humana reduzindo-a a um tecido imunologicamente não aceito.
Os agentes clareadores usados intracoronariamente, tais como o perborato de sódio associado com ao peróxido de hidrogênio, provocam aumento significante da permeabilidade dentinária (SAQUY et al, 1992) e redução da microdureza da dentina (CANEPA et al, 1993 e PÉCORA et al, 1994).
DAHLSTRON, em 1993, verificou que o peróxido de hidrogênio gera radicais hidroxila altamente reativos capazes de destruir componentes do tecido conjuntivo, colágeno e ácido hialurônico.
No que diz respeito aos agentes clareadores usados em dentes vitais, pesquisas são realizadas com o intuito de avaliar o que esses agentes causam às estruturas dentais.
Em 1981, SEALI et al relataram que o peróxido de hidrogênio a 30% causa mudanças destrutivas nos tecidos da polpa, favorecendo o aparecimento de reabsorções internas nos dentes vitais.
BOWLES & THOMPSON, em 1986, detectaram reação pulpar em dentes vitais clareados com peróxido de hidrogênio com ou sem aquecimento e que tais reações iam de simples processo inflamatório reversíveis até necrose pulpar. Esses autores também relataram que as enzimas pulpares são inibidas na presença do peróxido de hidrogênio, especialmente quando associado ao agente físico calor.
SEGHI & DENRY, em 1992, e SHANNON et al, em 1993, relataram que o agente clareador à base de peróxido de carbamida a 10% não alterava a microdureza do esmalte durante o clareamento de dentes vitais, mas observaram, por meio da microscopia eletrônica de varredura, modificações morfológicas do esmalte.
Atualmente
os pesquisadores estão preocupados em investigar como os agentes
clareadores utilizados em dentes vitais atuam sobre as estruturas dentais
e, assim, tentar obter um agente que promova o clareamento dental sem provocar
danos aos tecidos, se é que isso é possível.
O conhecimento científico da Odontologia evoluiu numa seqüência gradual, em ciclos ora lentos, ora rápidos, dependendo do espírito de cada época.
Muitos foram os profissionais que contribuíram marcadamente para o avanço científico em nossa profissão. Procuraremos citar, aqui, alguns que colaboraram no desenvolvimento das técnicas de clareamento dental. A citação de todos seria praticamente impossível, em virtude do grande acervo literário existente.
Assim, gostaríamos inicialmente de salientar os trabalhos pioneiros do professor MQUILLEN do Colégio Dental da Filadélfia, que, em 1861, escreveu na renomada revista especializada The Dental Cosmos. Em seu artigo, o autor comentava que o clareamento dental havia ocupado um bom espaço e chamado muita atenção na Convenção de New Haven, e que esse importante tema estava começando a ser discutido pelos profissionais da Odontologia, demonstrando uma evidência de progresso. Continuando, este eminente professor salientava que o primeiro passo era conhecer as características químicas das substâncias que alteravam a cor natural dos dentes, as quais deveriam ser decompostas para restabelecimento da normalidade. Demostrava assim que, sem o conhecimento da química, todo esforço seria empírico. Citava como agentes clareadores o SO2 e o Licor de Labarraque. Este último já havia sido relatado por Woodnutt (1860).
Em 1866, MQUILLEN publicou trabalho descrevendo um método para examinar as estruturas dentais pelo microscópio, demonstrando a presença de canalículos dentinários e sua extrema relação com o órgão pulpar. No ano seguinte, 1867, em outro artigo, ressaltava a característica de óxido-redução dos agentes clareadores de dentes escurecidos.
BOGUE (1872) e também Charple (1877) preconizavam o ácido oxálico como um agente que poderia ser usado no clareamento de dentes escurecidos pela penetração de sangue no interior dos canalículos dentinários.
TRUMAN (1881) relatou que utilizava o hipoclorito de cálcio com muito sucesso clínico, desde 1864 e salientava que o produto não era deletério às estruturas dentais.
KIRK (1893), com base no conhecimento do processo de óxido-redução, preconizou o uso do Na2O2 como um potente agente clareador de dentes escurecidos após o tratamento endodôntico.
Westlake (1895) utilizava corrente elétrica com pyrozone. O eletrodo positivo era colocado no dente e o eletrodo negativo na mão do paciente. Este método foi logo abandonado por ser considerado perigoso. O pyrozone consista em uma solução composta de cinco partes de peróxido de hidrogênio a 25% e uma parte de éter.
Kirk (1906) reforçou o conceito de que o problema fundamental do clareamento dental depende de uma reação química entre um composto corado e uma substância qualquer capaz de agir sobre a molécula corada e alterar sua cor. Para ele, o dióxido de sódio era a substância que deveria ser empregada no clareamento dental por ser um potente agente oxidante.
Ainda KIRK (1910), na terceirta edição de seu livro "Manuel de Dentisterie Operative", apresentou um capítulo bastante extenso dedicado ao clareamento de dentes escurecidos, relatando vasto conhecimento sobre a etiologia e técnicas de tratamento empregados naquela época.
GIBSON (1910) divulgou em seu trabalho que empregava agentes clareadores, tais como o Na2O2, o hipoclorito de cálcio e o pyrozone.
KERN (1910) relatou duas técnicas de clareamento: na primeira, ele empregava cristais de iodo e na segunda, o hipoclorito de cálcio.
Prinz (1924) citou uma técnica para clareamento de dentes escurecidos após o tratamento endodôntico onde se utilizava uma solução aquecida de perborato de sódio com peróxido de hidrogênio a 30% (Superoxolâ ). Esse autor aconselhava que o canal radicular deveria estar bem obturado antes de se iniciar o processo de clareamento. Nessa técnica, a câmara pulpar era limpa e lavada com a solução aquecida. Após isso o dente era seco e envolvido com algodão; gotejava-se a solução de peróxido de hidrogênio e se aquecia com o calor gerado por uma lâmpada, durante 15 minutos. Esse processo, segundo o autor, deveria ser repetido a cada dois dias, até se obter a cor desejada.
A proposta de PRINZ (1924) parece ser o primeiro relato onde um agente clareador era empregado sobre a estrutura do esmalte, uma vez que ele embebia toda a coroa do dente com algodão umedecido em peróxido de hidrogênio a 30% e usava calor como agente acelerador. Essa técnica sofreu várias transformações no decorrer do tempo mas, sem dúvida, foi uma das pioneiras no que diz respeito à termocatálise.
Buckley (1926) publicou tanto em seu livro intitulado "Materia Médica, Farmacologia y Terapeutica Dental", como em um capítulo no livro de JOHNSON (1927) "La Practica Odontológica", matéria sobre o clareamento de dentes escurecidos, demonstrando grande conhecimento sobre o assunto e descrevendo todas as técnicas preconizadas até aquela época. Esse autor, a quem a Odontologia deve muito, enfatizou que a melhor forma de clarear um dente é evitar o seu escurecimento. Essa idéia de Buckley é válida mas não é totalmente possível, uma vez que o escurecimento do dente ocorre por fatores que estão, muitas vezes, fora dos cuidados dos pacientes e profissionais.
AMES (1937), diante de um grande problema que atingia a população de sua região - a presença de dentes manchados por excesso de flúor na água, criou um método para clareamento dessas manchas. Assim, parece ser esse o primeiro método difundido para ajudar o clareamento de dentes manchados por fluorose. Em observações preliminares, ele constatou que 50% dos estudantes da Smithfield High School apresentavam esmalte manchado. A técnica apresentada consistia nos seguintes passos: a) isolamento do dente a ser tratado com dique de borracha; b) proteção de toda a face do paciente: c) aplicação de um rolo de algodão sobre o dentes em questão, que era embebido em uma solução preparada do seguinte modo: 5 partes de peróxido de hidrogênio a 30% com 1 parte de éter; d) uso de agente calor para acelerar a reação de liberação de oxigênio nascente. O autor observou que nem todos os casos apresentavam resultado satisfatório na primeira aplicação e sugeriu repetições de sessões de tratamento com intervalo de duas a três semanas entre elas. Este trabalho marca uma grande etapa para a Odontologia, uma vez que foi a primeira proposta de uma técnica consistente para clarear dentes vitais.
SALVAS (1938) propôs uma técnica de clareamento de dentes tratados endodonticamente com o uso de uma mistura de perborato de sódio e água destilada. A pasta formada era colocada e selada na câmara pulpar por vários dias, até a obtenção da cor desejada. O perborato de sódio é um pó branco, estável no estado seco e que, em contato com a água, decompõe-se em metaborato de sódio e peróxido de hidrogênio. Este último pode gerar radicais hidroxila e oxigênio nascente. O perborato de sódio fornece H2O2 em meio alcalino.
GROSSMAN (1946), um dos mais proeminentes pesquisadores da área da Endodontia, salientou que o dente pode perder a sua cor natural após a remoção do órgão pulpar pelo fato de ocorrer a desidratação das estruturas coronárias com a conseqüente perda da translucidez. Comenta, ainda, que a alteração da cor da coroa dental pode ser devido: 1) à decomposição dos tecidos pulpares; 2) ao uso de arsênico como agente desvitalizador; 3) à excessiva hemorragia durante a remoção da polpa; 4) aos medicamentos e 5) aos materiais obturadores de canais radiculares deixados no interior da câmara pulpar. Reforça, também, o fato de que o clareamento dental tem por objetivo a restauração da cor natural do dente pela descoloração da substância corante causadora do escurecimento, por meio de um potente agente oxidante ou redutor. Como agentes oxidantes mais utilizados, cita: pyrozone (H2O2 a 25% misturado com éter), Superoxol (H2O2 a 30%) e dióxido de sódio (Na2O2). Esses agentes são oxidantes diretos, uma vez que fornecem oxigênio nascente. Enfatiza que os hipocloritos são oxidantes indiretos. O autor reforça a idéia de que os oxidantes diretos devem ser preferidos, uma vez que promovem resultados melhores e de forma mais rápida. No que diz respeito à técnica de clareamento, o autor cita o uso de peróxido de hidrogênio a 30% (Superoxol), associado à uma fonte de calor produzida por uma lâmpada elétrica.
O peróxido de uréia (peróxido de carbamida) foi introduzido na Endodontia em 1951, quando Blechman & Cohen pesquisaram sua capacidade de limpeza dos canais radiculares. O grande problema encontrado por esses autores consistia em encontrar um veículo satisfatório para a dissolução desse produto. O veículo não poderia ser a água, uma vez que esse peróxido decompõe-se nesse meio.
Cobe (1960) analisou a ação do peróxido de hidrogênio a 3% e do peróxido de uréia dissolvido em glicerina anidra (Gly-Oxideâ ) em presença de sangue humano. Os resultados obtidos evidenciaram que o peróxido de uréia, além de ter uma ação mais ativa, é também mais estável à temperatura ambiente, isso porque a quebra da ligação molecular desse peróxido é mais lenta quando comparada com a do peróxido de hidrogênio a 3% (água oxigenada 10 v).
Stewart et al (1961) avaliaram a capacidade do peróxido de uréia a 3% (Gly-Oxideâ ), da soda clorada e da água oxigenada no tratamento dos canais radiculares. Os autores admitiram que, possivelmente, o Gly-Oxideâ apresenta maior ação microbiana e melhor efeito sobre a limpeza dos canais radiculares. A solução de peróxido de uréia, ao reagir com a soda clorada (hipoclorito de sódio a 5%), produz efervescência e facilita a remoção de debris do interior do canal radicular.
Spasser (1961) reforçou a idéia de Salvas (1938), que preconizava o uso do perborato de sódio associado com água destilada e recomendava que a câmara pulpar deveria ser preparada para receber o agente clareador, ou seja, ela deveria estar isenta de qualquer material e ser lavada com solventes, tais como éter, clorofórmio ou álcool. A seguir, uma pasta formada com a mistura perborato de sódio e água destilada era colocada na câmara pulpar e aí permanecia por vários dias. O autor recomendava o cimento fosfato de zinco como selador provisório. Este procedimento deveria ser repetido a cada quatro dias.
NUTTING & POE (1963), com base no trabalho de SPASSER (1961), substituíram a água pelo peróxido de hidrogênio a 30% (Superoxolâ ). Essa associação somava o efeito de dois potentes agentes oxidantes, apresentando, assim, resultados clínicos mais rápidos.
MAISTO (1967), em seu famoso livro "Endodoncia", que serviu de base para muitos endodontistas brasileiros, não apresentou nada de novo no que tange ao clareamento dental, uma vez que cita uma técnica muito semelhante à de GROSSMAN (1946).
Stewart et al (1969), aproveitando as características quelantes do EDTA e as propriedades antissépticas do peróxido de uréia, preconizaram uma nova solução auxiliar de instrumentação, com a consistência de um creme (RC-Prepâ ). Esse creme é introduzido no interior da câmara pulpar e, sobre ele, adicionada soda clorada. Disso resulta uma reação de efervescência, com liberação de oxigênio nascente.
Uma vez que o peróxido de uréia (carbamida) está presente no creme proposto por STEWART et al (1969), esse produto também poderia ser testado como agente clareador. Parece haver falta de pesquisa sobre o assunto, pois não há citações na literatura revista.
CORCORAN & ZILLICH (1976) apresentaram um caso clínico de clareamento de dentes vitais manchados por tetraciclina. Eles utilizaram como agente clareador o Superoxolâ (H2O2 30%) e uma fonte que gerava calor (71 ° C) por um tempo de 20 minutos. Os autores utilizaram duas sessões com intervalo de uma semana entre elas.
HARRINGTON & NATKIN (1979) estudaram o efeito deletério do peróxido de hidrogênio a 30% e aventaram a hipótese de que esse produto poderia passar através da dentina e causar as reabsorções externas.
Preocupados com o efeito dos tratamentos clareadores para dentes vitalizados sobre a polpa, COHEN & CHASE (1979) avaliaram histologicamente 51 dentes humanos vitais, submetidos ao procedimento clareador com o uso da técnica de termocatálise com peróxido de hidrogênio a 30%. Os autores aplicaram o agente clareador nas coroas de pré-molares que foram depois extraídos por razões ortodônticas. O tratamento foi realizado em três sessões, com tempo de aplicação de trinta minutos cada. Os dentes foram extraídos após intervalos de uma hora, três dias, quinze dias e trinta dias. As observações histológicas demonstraram que essa técnica de clareamento para dentes vitais era inofensiva ao tecidos pulpares.
Em trabalho contraditório ao anterior, Robertson & Melfi (1980) realizaram uma pesquisa e concluíram que o uso do peróxido de hidrogênio a 30% associado ao calor provoca resposta inflamatória do órgão pulpar.
SEALI et al (1981), ao estudar polpas de cães expostas à ação do peróxido de hidrogênio a 30%, observaram mudanças destrutivas com formação de odontoclastos e lesões de reabsorções internas.
Howell (1981), em seu estudo sobre o clareamento dental, concluiu que cerca de 50% dos dentes submetidos a essa terapia apresentam regressão de cor após um ano. Ele reforçou o fato de que os dentes que mais demoraram para clarear foram os que mais rapidamente escureceram de novo.
A reversibilidade da cor dos dentes clareados pode ocorrer, pois a reação de clareamento dental consiste em um problema químico de óxido-redução e não na remoção do pigmento corante do interior das estruturas dentais. O agente clareador apenas transforma a substância corada em uma substância sem cor.
Essas observações despertaram os pesquisadores para analisar, cada vez mais, as ações deletérias dos potentes agentes clareadores sobre os tecidos dentais. Assim, LADO et al (1983) demostraram em suas pesquisas que o peróxido de hidrogênio a 30% desnaturava a dentina humana e tornava este tecido imunologicamente não aceito pelo organismo.
FRANK (1982), expõe no capítulo "Branqueamento de dentes polpados e despolpados" do livro "Caminhos da Polpa" (COHEN & BURNS, 1982), que utilizava, para o clareamento de dentes despolpados, a técnica de NUTTING & POE (1963): peróxido de hidrogênio a 30% misturado com perborato de sódio. Para os dentes polpados (vitais), o autor recomendava o uso da técnica da termocatálise, onde o peróxido de hidrogênio a 30% é colocado em uma bolinha de algodão sobre a estrutura de esmalte, que recebe a ação de calor emitida por uma lâmpada elétrica (32º C), por um tempo de 30 minutos. Esse autor salienta que, antes do procedimento do clareamento, o esmalte dental pode ser submetido à ação de ácido clorídrico a 10% ou de ácido fosfórico a 50%, por um tempo de 1 minuto, com o objetivo de favorecer o clareamento dental.
Lado et al (1983) salientaram que o paciente deve ser esclarecido sobre o prognóstico do clareamento e que o profissional não pode deixar de explicar a possibilidade de ocorrer reabsorções externas. Esses autores, ainda, chamam atenção dos profissionais para acompanhar por vários anos os dentes clareados, uma vez elas podem ocorrer no espaço de 1 a 7 anos. Eles relataram que a regressão de cor pode ocorrer em 4 por cento dos dentes submetidos ao clareamento.
GOON et al (1986) e LATCHAN (1986) publicaram casos clínicos associando o clareamento de dentes despolpados à alta incidência de reabsorções cervicais externas das raízes.
BOWLES & THOMPSON (1986) estudaram o efeito do calor e do peróxido de hidrogênio a 30% , isolados ou associados, sobre as enzimas da polpa de bovinos e observaram que o calor e o peróxido de hidrogênio a 30% apresentavam efeitos destrutivos sobre essas enzimas. Porém, o calor apresentou menor efeito destrutivo que o peróxido de hidrogênio a 30%.
BOWLES & UGWUNERI (1987) realizaram uma investigação onde detectaram uma quantidade de peróxido de hidrogênio que alcançava a câmara pulpar durante o clareamento dental. No interior da câmara pulpar, eles colocaram uma solução tamponada com pH 4,5 e, na superfície do esmalte, peróxido de hidrogênio a 1, 10, e 30 por cento à temperatura de 37oC por 15 minutos. Após esse tempo, a solução tamponada era examinada por meio de colorímetro. Os resultados evidenciaram que uma significante quantidade de peróxido de hidrogênio atingia a câmara pulpar e sua concentração era aumentada pela elevação da temperatura.
Nathanson & Parra (1987) descreveram um processo de clareamento térmico no qual o esmalte era condicionado, após o que o peróxido de hidrogênio a 35% era aplicado e aquecido com o emprego de uma luz colocada a aproximadamente 13 polegadas do dente a ser clareado. A temperatura era controlada por um reostato. Os autores concluíram que, para a eficiência deste processo, o tempo de exposição da solução clareadora ao calor deveria ser de 30 minutos.
A reabsorção cervical da raiz tem sido atribuída à natureza tóxica do peróxido de hidrogênio, que pode difundir-se através da dentina e atingir os tecidos periodontais (Friedman et al, 1988; Dahlston, 1993).
TITLLEY et al (1988) observaram, por meio de microscopia eletrônica de varredura, que a aplicação de ataque ácido na dentina promove a abertura dos canalículos dentinários e aumenta a permeabilidade desse tecido favorecendo a passagem do peróxido de hidrogênio a 30% .
Friedman et al (1988) fizeram um acompanhamento de 56 dentes clareados por um período longo. Eles observaram que as reabsorções externas apareceram em 6,9% dos casos. Quanto ao fator estético, observaram que 50% apresentaram-se aceitáveis e 21% apresentaram fracasso.
Observa-se que, até a década de 80, muitas pesquisas foram realizadas na tentativa de se obterem técnicas de clareamento de dentes vitais mais eficientes. Porém, todas utilizavam o peróxido de hidrogênio altamente concentrado como solução ativa, o que forçava a participação direta do cirurgião-dentista na aplicação desse produto.
A grande novidade surgiu quando HAYWOOD & HEYMANN (1989) propuseram uma técnica revolucionária, apresentando como agente clareador de dentes vitais um gel cuja substância ativa era o peróxido de carbamida a 10% (peróxido de uréia).
A técnica proposta pelos autores supracitados consiste no seguinte: a) o profissional deve realizar uma profilaxia nos dentes de seu paciente; b) moldar a arcada ou arcadas com alginato; c) com o modelo obtido, preparar alívios nos locais dos dentes onde será aplicado o gel clareador e , a seguir, confeccionar uma moldeira de plástico termoformável em um termoplastificador à vácuo; d) adaptar a moldeira obtida de modo que o paciente sinta-se confortável ao usá-la; e) orientar o paciente a colocar nos lugares da moldeira correspondente aos dentes que serão clareados, uma ou duas gotas do gel clareador; f) ensinar o paciente a colocar a moldeira na arcada e orientá-lo para remover o excesso de gel, de modo que o paciente não o degluta; g) orientar o paciente de modo que fique com a moldeira em sua boca durante toda a noite; h) no dia seguinte, o paciente deve remover a moldeira e escovar bem os dentes; i) repetir a aplicação todas as noites, até que o profissional indique a interrupção do tratamento. Esses autores salientaram que o profissional deve supervisionar o tratamento, vendo o paciente periodicamente. Salientam, ainda, que essa técnica é uma alternativa ao clareamento de dentes vitais que deve ser a de primeira escolha, por ser menos agressiva e promover um clareamento de forma lenta e gradual.
McEvoy (1989) indicou o ácido clorídrico a 18% como efetivo na remoção de manchas superficiais de esmalte relacionados à fluorose dental. A vantagem de sua utilização seria a remoção permanente de uma camada superficial de esmalte, expondo as manchas ao tratamento clareador. Manchas mais profundas, em dentina, não poderiam ser clareadas. O autor ainda relatou que o peróxido de hidrogênio poderia ser utilizado nestes casos e que sua ação seria melhorada pelo aquecimento. Enfatizou que somente o peróxido de hidrogênio seria adequado à remoção de manchas de tetraciclina e que o sucesso do tratamento estaria na dependência da idade do paciente, da tonalidade e localização das manchas.
COVINGTON et al (1990) examinaram o efeito do peróxido de carbamida sobre a composição química e a superfície do esmalte humano. A investigação desses autores foi realizada in vitro com dentes extraídos que, em suas superfícies, era colocado gel de peróxido de carbamida por um tempo de três semanas, de modo o gel era substituído a cada quatro horas. Uma área da superfície do esmalte era utilizada para controle. Decorrido o tempo experimental, com auxílio de um microscópio eletrônico de varredura, eles observaram que a superfície submetida à ação do gel clareador apresentava-se com erosão, fato que não estava presente antes da ação do produto. A análise química das áreas submetidas a ação dos agente pesquisado demonstrou perda dos componentes orgânicos do esmalte. Esses autores ressaltaram que o gel peróxido de carbamida fornece peróxido de hidrogênio, que tem sido associado à presença de inflamação crônica, hipersensibilidade dental e, em altas concentrações, à lesões neoplásicas.
HAYWOOD (1990) avaliou o efeito do peróxido de carbamida a 10% sobre a superfície do esmalte. Dentes extraídos foram submetidos à ação do agente clareador por um período equivalente a 5 semanas com aplicação noturna. Uma área controle foi utilizada em cada dente, por meio da selagem de uma certa parte do esmalte. Nenhum dos dentes submetidos ao processo de clareamento apresentou alteração aparente de sua estrutura, detectável ao microscópio eletrônico de varredura.
ROTSTEIN et al (1991), preocupados com o clareamento dental intracoronário, investigaram a eficácia do agente perborato de sódio associado com peróxido de hidrogênio a 30%, a 3% e com água, no clareamento dental. Esse estudo foi realizado in vitro, em dentes previamente escurecidos. Essas associações, que correspondem a três grupos, foram colocadas nas câmaras pulpares dos dentes e trocadas após 3, 7, e 14 dias. Os resultados possibilitaram a conclusão que as três associações eram igualmente eficazes e os autores, então, reforçaram a idéia de que o uso do perborato de sódio misturado com água deveria ser preferível aos demais, uma vez que não causa problemas de reabsorções cervicais externas das raízes, quando utilizado em pacientes.
HAYWOOD & HEYMANN (1991) realizaram uma revisão de literatura onde salientavam que a técnica de clareamento de dentes vitais conhecida como Nigthguard, cujo principal componente ativo é o peróxido de carbamida a 10%, era segura para os pacientes, desde que fosse executada de modo correto e sob a supervisão do profissional responsável.
LeVinh (1991) questionou a segurança dos clareadores dentais noturnos, nos quais o peróxido de carbamida fica em contato com tecidos bucais durante muito tempo. Segundo esse autor o peróxido de carbamida tem propriedades mutagênicas e cancerígenas. Assim, desencorajou o uso indiscriminado desse agente clareador, até que estudos de longo prazo sejam feitos.
Wong & Schmidt (1991) descreveram um caso clínico em que um incisivo central superior com alteração de cor foi tratado com sucesso utilizando a técnica termocatalítica de clareamento vital, utilizando o agente peróxido de hidrogênio a 30%.
Hall (1991) avaliou a influência do condicionamento ácido em dez pacientes. Para isso os pacientes tiveram seus dentes de um lado condicionados com ácido, enquanto que, no outro hemi-arco, o condicionamento foi omitido. Os resultados evidenciaram que não houve diferenças significantes que justificassem o condicionamento ácido prévio ao emprego da técnica de clareamento de dentes vitalizados com peróxido de hidrogênio.
Preocupados com a segurança da saúde dos pacientes, RITTER et al (1992) relataram que, apesar dos agentes clareadores para dentes vitais disponíveis no mercado não terem a aceitação definitiva da American Dental Association (ADA), o peróxido de carbamida (10 a 15%) e o peróxido de hidrogênio (1,5 a 3%) são reconhecidos pela Food and Drug Administration (FDA) como produtos seguros e eficazes para tratar lesões da mucosa bucal. Os autores ressaltam que o clareamento de dentes vitais, realizado em consultório, emprega o peróxido de hidrogênio (30-35%) e que as técnicas conhecidas como Nigthguard ou Caseira utilizam o peróxido de carbamida. Esta última técnica apresenta para o paciente um custo menor, por ser auto-administrada e diminuir o tempo de atuação do profissional. Esses pesquisadores mostraram suas preocupações com as técnicas que utilizam peróxido de uréia, uma vez que esse produto degrada-se em peróxido de hidrogênio (3 a 5%) e uréia (7 a 10%). O peróxido de hidrogênio gerado decompõe-se em oxigênio livre e água e a uréia em amônio e dióxido de carbono, que são tóxicos ao organismo.
PÉCORA et al (1991), preocupados com a passagem do peróxido de hidrogênio a 30% através dos canalículos dentinários, aventada por HARRINGTON & NATKIN (1979) e TITLLEY et al (1988), desenvolveram in vitro um método químico capaz de revelar a passagem dessa solução através da dentina, no terço cervical da raiz dos dentes tratados endodonticamente, submetidos à ação deste potente agente clareador.
Rotstein et al (1991) investigaram, em pré-molares extraídos e com canais tratados, a penetração do peróxido de hidrogênio a 30% como agente clareador intracoronário em função do tempo e da temperatura de aplicação. Estudaram em um tempo de 5, 20, 40 e 60 minutos, com as temperaturas de 24, 37 e 45 graus centígrados. Os resultados evidenciaram uma relação direta entre o tempo e a penetração do agente clareador. Os autores recomendaram a utilização do H2O2 a 30% durante o menor tempo e na temperatura mais baixa possível.
SCHERER et al (1991) realizaram investigações na superfície do esmalte humano, por meio da microscopia eletrônica de varredura, após a aplicação dos géis clareadores à base de peróxido de carbamida por um tempo de 5, 15 e 30 dias, constatando que, após trinta dias, o esmalte apresentava-se com alterações em sua superfície.
POWELL & BALES (1991), após uma extensiva revisão de literatura sobre os agentes clareadores de dentes vitais, recomendaram: a) o uso de dique de borracha ao se utilizar agentes altamente concentrados; b) evitar o contato dos agentes com a mucosa bucal, mesmo que sejam de baixa concentração; c) usar agentes clareadores por um tempo menor possível e sem aumento de temperatura para não alterar a vitalidade pulpar; d) examinar com muita atenção a estrutura de esmalte para verificar se não há presença de trincas e dentina exposta; e) avisar o paciente sobre a possibilidade de ocorrer sensibilidade dental após o procedimento de clareamento; f) evitar aplicar os agentes clareadores nas áreas cervicais com o intuito de não causar reabsorções e g) não aplicar agente clareador em áreas onde o esmalte esteja muito fino.
CHRISTENSEN (1991), em seu artigo "Clarear ou não clarear" salientou que o conceito de clareamento caseiro com peróxido de carbamida havia sido introduzido há dois anos e meio e foi prontamente aceito pelos pacientes e profissionais de modo muito mais rápido do que qualquer conceito na história da Odontologia. Salientou, também, que foi aceito sem que pesquisas mais apuradas houvessem sido realizadas e comentou que seu sucesso deveu-se ao fato de ser mais econômico, realizado pelo paciente, sem qualquer dor e estresse de consultório e, ainda, sem tomar tempo do cirurgião-dentista.
Seghi & Denry (1992) avaliaram o efeito de um gel à base de peróxido de carbamida a 10% (White Briteâ ) sobre a microdureza e a característica de abrasão do esmalte humano. Os resultados mostraram que a força necessária para fraturar o esmalte era 30% menor, sem alterar a microdureza, e que a aplicação do gel diminuiu a resistência à abrasão do esmalte humano. Esse comportamento, segundo os autores, estava relacionado com a alteração da matriz orgânica do esmalte sob ação do peróxido de hidrogênio.
GLICKMAM et al (1992) relataram um caso clínico de flare up após a aplicação de agente clareador em dente vital. Eles utilizaram a solução Star Briteâ (H2O2 a 35%) misturada a um agente em forma de gel e aplicaram em toda a superfície coronária durante 20 minutos. Após 24 horas, o paciente retornou ao consultório com dor severa, associada a edema. O caso ilustra a importância de um apurado exame das condições pulpares e periodontais antes de o dente ser submetido a procedimentos clareadores.
Saquy et al (1992) verificaram a ação de associações de perborato de sódio com peróxido de hidrogênio com ou sem aplicação de calor sobre a permeabilidade dentinária. A identificação da permeabilidade foi detectada por meio da infiltração de ions cobre e a quantificação foi feita por meio da análise morfométrica. Os resultados evidenciaram que a associação de perborato de sódio com peróxido de hidrogênio a 30% aumenta a permeabilidade dentinária, e a adição de calor à essa associação provoca aumento acentuado da permeabilidade.
BOWLES & BURNS (1992) investigaram se a polpa dental exibia alguma ação de catalase ou peroxidase que a protege dos efeitos deletérios dos agentes oxidantes durante o clareamento dental. O tecido pulpar de dentes humanos saudáveis tiveram suas atividades de catalase e peroxidase analisadas. A taxa de quebra do peróxido de hidrogênio pelo tecido pulpar foi medida. A atividade de catalase é definida em m M de peróxido de hidrogênio quebrado por minuto e miligrama do tecido. Os resultados indicaram que o tecido pulpar exibia uma atividade de catalase muito baixa. Assim, os autores chamam atenção para o fato de que os agentes clareadores à base de peróxido devem ser utilizados com muito cuidado e com a supervisão do cirurgião-dentista.
BITTER (1992) avaliou o efeito de três produtos comerciais à base de peróxido de carbamida utilizados como clareadores para dentes vitais (Rembrandt Lightenâ , Ultra Briteâ e Natural Whiteâ ) sobre a superfície do esmalte após um tempo de aplicação de 30 horas. O microscópio eletrônico de varredura evidenciou que esses produtos aumentavam a porosidade do esmalte e que as alterações não eram uniformes.
Rotstein et al (1992) estudaram o efeito de agentes clareadores sobre os componentes inorgânicos da dentina e do cemento humano. Os autores constataram que o H2O2 a 30% aumentava significante a solubilidade da dentina e do cemento. Verificaram também que o aumento da dissolução está em função do tempo e o máximo ocorre após 72 horas de aplicação.
HAYWOOD (1992) realizou uma revisão de literatura sobre o uso de agentes clareadores e verificou que o peróxido de hidrogênio a 30% é utilizado tanto para clarear dentes vitais como dentes tratados endodonticamente. O peróxido de carbamida a 10% em forma de gel tem sido indicado em muitas técnicas de clareamento de dentes vitais. Esse autor também salienta que o peróxido de carbamida degrada em 3% de peróxido de hidrogênio e 7% de uréia e se pode considerar que o agente ativo é o peróxido de hidrogênio. O autor chama atenção para o fato de o peróxido de hidrogênio ser bacteriostático e, em alta concentração, mutagênico.
HELLER et al (1992) investigaram histológica e radiograficamente a ação do agente clareador mistura de perborato de sódio com peróxido de hidrogênio a 30%, associado ao calor, sobre a superfície cervical radicular e tecidos periodontais em dentes de cães tratados endodonticamente. Em um grupo, não se utilizou agente clareador para servir de controle. Os animais tiveram seus dentes radiografados e foram sacrificados com intervalos de um a três meses após a aplicação da solução testada. Reabsorções externas das raízes foram observadas, histologicamente, nos dentes após três meses.
COOPER et al (1992), preocupados com a ação do peróxido de carbamida e de hidrogênio em dentes vitais, verificaram sua penetração através do esmalte, passando pela dentina até atingir a câmara pulpar, trabalhando com dentes extraídos. Eles aplicaram gel de peróxido de carbamida na superfície de esmalte e captaram sua presença na câmara pulpar por meio de uma solução reveladora de leuco cristal violeta. A quantidade de peróxido encontrado na câmara pulpar, após 15 minutos de aplicação desses géis à temperatura de 37°C, foi de 3,3 µ g de peróxido de carbamida a 10% e de 40,4 µ g de peróxido de hidrogênio a 30%. Assim, o trabalho elucidou a passagem desses peróxidos através das estruturas dentais, dando mais conhecimento sobre o assunto, abrindo novas perspectivas para investigações do efeito desses peróxidos sobre o tecido pulpar.
Canepa et al (1993) verificaram que a associação do perborato de sódio com o peróxido de hidrogênio a 30%, somado à ação do calor, promove redução na microdureza da dentina humana, e que essa microdureza é reduzida cada vez mais à medida que se repete a aplicação desses agentes clareadores.
Dahlston (1993) clareou intracoronariamente 204 dentes (Adelaide-Australia) e constatou reabsorção cervical externa em 1,96%. O autor relacionou essa reabsorção ao uso do peróxido de hidrogênio a 30%. Esses dados foram bem menores que os encontrados por Friedman et al (1988), que foi de 6,8%. Ele observou que o peróxido de hidrogênio gera radicais hidroxila na presença de sais de ferro e constatou uma significante associação entre a produção desses radicais e a presença de dentes com alteração de cor causada por sangue, em dentes tratados endodoticamente, que foram clareados pelo método termocatalítico (H2O2 + calor). Continuando, o autor relatou que o desenvolvimento de alteração profunda de cor tem sido atribuída ao extravasamento de componetes do sangue da câmara pulpar para os canalículos dentinários, com subseqüente decomposição. A quebra de eritrócitos libera ferro e a combinação desses ions ferro com o sulfeto de hidrogênio produzido por bactérias pode também resultar na formação de sais de ferro (sulfeto de ferro), alterando a cor no dente.
TONG et al (1993) estudaram os efeitos das técnicas de clareamento microabrasivas de dentes vitais sobre o esmalte dental. Os espécimes tratados somente com ácido fosfórico a 37% mostraram a perda de 5,7 m m de esmalte. Os espécimes tratados com aplicação prévia de ácido fosfórico a 37% e com posterior ação do peróxido de hidrogênio a 30% tiveram perda de 5,3 m m. A aplicação direta de ácido clorídrico a 18% resultou na perda de 100 m m de esmalte. A aplicação do ácido clorídrico a 18% com pedra pomes ocasionou perda de 360 m m de esmalte. Esses autores ressaltaram que o uso do ácido clorídrico a 18% e pedra pomes com o uso de instrumentos rotatórios contribuíram marcadamente para a perda da estrutura do esmalte. Eles chamam atenção para o fato de a técnica com ácido clorídrico misturado com pedra pomes ser muito difundida entre os dentistas, sendo necessária maior precaução.
SHANNON et al (1993) avaliaram o efeito de três géis clareadores à base de peróxido de carbamida a 10% (Proxigelâ , Rembrandtâ e Gly-Oxideâ ) sobre a microdureza do esmalte e sua superfície morfológica. Eles não encontraram diferença estatística na microdureza Vickers utilizando carga de 400 gramas; porém, observaram, por meio de microscopia eletrônica de varredura, alterações significantes na superfície do esmalte submetido à ação dos géis clareadores.
BISHARA et al (1993) analisaram o efeito do gel peróxido de carbamida sobre a colagem dos brackets utilizados em Ortodontia e, com base em seus experimentos com força de tração, verificaram que esse agente clareador não interferia na adesão dos referidos dispositivos ortodônticos.
ROTSTEIN et al (1993), preocupados com os efeitos deletérios do peróxido de hidrogênio a 30% sobre as estruturas dentinárias e tecidos periodontais, provocando as reabsorções externas, reforçaram a orientação de que se deve preferir o perborato de sódio misturado com água como agente clareador de dentes tratados endodonticamente.
CHERRY et al (1993) conduziram um estudo com o objetivo de determinar se a ingestão de produtos clareadores contendo peróxido de carbamida apresentava efeito tóxico. Eles utilizaram ratas fêmeas adultas e lhes aplicaram gel clareador na quantidade de 5 gramas por quilo de peso do animal. Os ratos controles receberam água deionizada. Os resultados evidenciaram que o gel Quik Startâ (peróxido de carbamida a 35%) ingerido pelas ratas promoveu diminuição do ritmo respiratório de 169 para 55, a temperatura corporal diminuía de 38,4 para 34oC. Dos animais examinados, três morreram antes de decorrer 48 horas de ingestão do produto, por hemorragia gástrica. Dez ratas tiveram ovulação interrompida e três ratas apresentaram necrose na mucosa bucal. Os animais que ingeriram os géis White & Briteâ ou Nu-Smileâ (peróxido de carbamida a 10 e 15%, respectivamente) apresentaram os mesmos sintomas, porém de forma mais suave. Não foi observada morte com o uso dessas concentrações. O trabalho conclui que esses agentes clareadores à base de peróxido de carbamida eram tóxicos aos animais testados.
O trabalho de CHERRY et al (1993) abre um perspectiva muito séria, pois os profissionais de Odontologia necessitam, urgentemente, saber que efeito tem, no humano, a ingestão de peróxido de carbamida, uma vez que o clareamento dental caseiro está sendo cada vez mais difundido, por um tempo sem controle. A ingestão diária e prolongada deste produto deve ser mais investigada. A técnica de clareamento pode produzir bom resultado estético, mas é dever dos cirurgiões-dentistas ter um conhecimento científico bastante claro a seu respeito, para não provocar danos à saúde dos pacientes.
VIEIRA et al (1993), preocupados com a parte técnica, preconizaram, para o clareamento de dentes manchados por tetraciclina, um procedimento onde tomavam o cuidado de proteger áreas do dente não afetadas, de modo que o agente clareador atuasse somente nas áreas manchadas. O agente recomendado por esses autores é um gel à base de peróxido de carbamida.
KWONG et al (1993) avaliaram clínica e histologicamente a ação gel Carbaliteâ no clareamento de dentes vitais. A composição química do produto testado era a seguinte: peróxido de carbamida a 10% com glicerina. Pacientes voluntários foram utilizados neste experimento. O agente foi utilizado por 2 semanas. Os pacientes relataram que o produto apresentava um sabor amargo adocicado e não acusaram nenhuma sensibilidade nos dentes durante a fase de tratamento. Os resultados histológicos dos dentes extraídos desses pacientes mostrou que, em dois dos seis dentes extraídos após dois dias de aplicação do gel e em três dentes dos sete extraídos após duas semanas de aplicação, encontrou-se polpa com moderada resposta inflamatória. Essas respostas inflamatórias estavam todas localizadas adjacentes à camada dos odontoblastos. Os vasos sangüíneos estavam dilatados, com presença de linfócitos. Nos dentes avulsionados após duas semanas de tratamento, o exame histológico mostrava predominância de neutrófilos polimorfos e a camada de odontoblastos estava intacta em toda as secções examinadas. Não se detectou alteração na estrutura de dentina. Os dentes controles apresentavam-se normais. Os autores, com vistas nesse experimento, chamaram atenção para a necessidade de novas investigações sobre a ação das soluções à base de peróxido de carbamida sobre a polpa dos dentes humanos.
HAYWOOD (1993) comenta que há três classes de materiais e técnicas utilizadas para clareamento de dentes vitais, tais como: o clareamento realizado em consultório com a aplicação do peróxido de hidrogênio a 30%, a técnica Nightguard com peróxido de carbamida em forma de gel e a técnica que utiliza gel de peróxido de hidrogênio com concentração que pode variar de 3 a 6%. Comenta, ainda, que a técnica mais popular é a Nightguard, conhecida como técnica de clareamento caseiro. O autor procura esclarecer que a técnica Nightguard deve ser utilizada para clarear dentes escurecidos pela idade e os dentes manchados pela ingestão de tetraciclina durante sua formação. Salienta, também, que o clareamento satisfatório pode ocorrer entre duas a três semanas de aplicação e em casos mais severos, entre três e quatro meses.
KILLIAN (1993) relatou um caso clínico de fluorose dental clareado pela técnica Nightguard com o uso de agente clareador à base de peróxido de carbamida. O autor não citou nem a marca e nem a concentração utilizada.
Pécora et al (1994) verificaram a diminuição da dureza da dentina humana após aplicações de agentes clareadores por 72 horas. Os agentes clareadores utilizados foram perborato de sódio + água, perborato de sódio + peróxido de hidrogênio a 3%, perborato de sódio + peróxido de hidrogênio a 30%, Endoperoxâ (peróxido de hidrogênio cristalizado), Proxigelâ (peróxido de carbamida a 10%) e peróxido de hidrogênio a 30%. As misturas de perborato de sódio + água e perborato de sódio + peróxido de hidrogênio a 3% promoveram a menor diminuição da dureza da dentina. Os agentes perborato de sódio + peróxido de hidrogênio a 30%, Endoperoxâ e peróxido de carbamida a 10% proporcionaram maior diminuição da dureza da dentina. O agente peróxido de hidrogênio a 30% reduz acentuadamente a microdureza da dentina. Todos os agentes clareadores estudados por esses autores promoveram redução da microdureza da dentina e, portanto, cabe aos pesquisadores investigarem um agente oxidante ou um agente redutor que não tenha efeito deletério sobre a estrutura de dentina.
BARRIENTOS et al (1994) examinaram, por meio de cortes histológicos, coroas de dentes extraídos portadores de tratamento endodôntico e diferentes tipos de pigmentações intrínsecas com mais de 10 anos, causadas por hemorragias, necrose pulpar e medicamentos. Eles utilizaram uma coroa dental sem pigmentação como controle. Os achados histológicos evidenciaram que os pigmentos se concentravam não somente no interior dos canalículos dentinários, como também na substância intercanalicular e nas zonas interglobulares. Os autores salientaram que tais fatos poderiam explicar a dificuldade de clareamento quando da utilização do peróxido de hidrogênio.
SCHULTE et al (1994) avaliaram e compararam a resposta de vitalidade pulpar ao uso do peróxido de carbamida a 10%, marca Opalescenceâ , aplicado em pacientes voluntários, sendo 16 do sexo masculino e 12 do sexo feminino, com idade média de 26 anos. O teste elétrico foi utilizado para detectar a vitalidade. Dos pacientes observados, apenas 4 acusaram aumento da sensibilidade pulpar. Os demais não apresentaram qualquer mudança.
FRYSH et al (1995) estudaram, de modo comparativo, a ação do peróxido de hidrogênio com pH 4,4 (ácido) e com pH 9,0 (básico) quanto à capacidade de clarear dentes escurecidos. O estudo in vitro esclareceu que o peróxido de hidrogênio básico é mais efetivo que o ácido. Segundo os autores, este aumento da eficácia pode permitir ao dentista obter resultado de clareamento em tempo bem mais reduzido e, assim, reduzir o risco de causar danos tanto aos dentes como às estruturas dos tecidos moles.
CURTIS JR et al (1995) avaliaram o efeito de um método que deve ser supervisionado pelo dentista e aplicado ao paciente que está submetido ao tratamento de clareamento de dentes vitais com peróxido de carbamida a 10%. O sulco epitelial, a gengiva marginal, os tecidos adjacentes e outras regiões da mucosa bucal sofrem ação dessa solução de modo bastante sutil. O método apresentado serve para detectar clinicamente essas reações adversas.
McEVOY (1995) cita que, para as remoções da manchas intrísecas de dentes vitais, são usadas as técnicas microabrasivas (ácido clorídrico), técnicas termocatalíticas (peróxido de hidrogênio a 30% + calor) e a técnica de clareamento caseiro (peróxido de carbamida). O autor comenta que, se as técnicas forem associadas, os resultados serão obtidos de forma mais rápida.
DAHL & BECHER (1995) investigaram o efeito tóxico do peróxido de carbamida puro e em forma de gel aplicados em ratos. Injetaram 5, 15 e 50 mg de peróxido de carbamida puro e em forma de gel no estômago dos ratos. Os animais foram sacrificados decorridas 1 e 24 horas após a ingestão do produto. O exame histológico revelou ulcerações no estômago desses animais quando a eles era aplicado o produto em forma de gel. Esse fato pode ser atribuído ao carbopol, veículo espessante, que adere nas paredes do estômago e libera oxigênio lentamente. Os autores não encontraram danos aparentes no fígado e rins. Eles chamaram atenção para o fato, pois quando da aplicação em pacientes, o gel permanece por longo período na cavidade bucal, podendo ser ingerido em parte e causar danos à sua saúde.
Citar todos os trabalhos que foram publicados sobre as variações de técnicas de clareamento de dentes escurecidos, quer por razões extrínsecas, quer por manchas intrísecas de dentes vitais, seria uma tarefa não só impossível, como também repetitiva, uma vez que as técnicas difundidas pelos clínicos e pesquisadores não diferem muito em seus procedimentos básicos.
Procurou-se, neste capítulo, centralizar atenção sobre os trabalhos pioneiros, aqueles que desenvolveram técnicas tanto para clarear dentes despolpados como vitais. Deu-se especial destaque aos trabalhos de investigação científica, que procuraram analisar as ações físico-químicas dos agentes clareadores, suas ações sobre as estruturas dentais e seus efeitos deletérios sobre a saúde geral do paciente.
Sabe-se
que o ideal não é atingível, mas não procurá-lo
seria perder o sonho e a esperança de um mundo melhor.
O clareamento de dentes vitais está cada vez mais difundido, principalmente, o método de aplicação de géis clareadores pelo próprio paciente, com a supervisão do cirurgião-dentista.
A
literatura consultada evidenciou poucos estudos sobre a ação
dos agentes clareadores à base de peróxido de carbamida sobre
a estrutura do esmalte humano. Assim, o presente trabalho tem por objetivo
estudar a ação desses géis sobre a microdureza dessa
estrutura anatômica.
Para o estudo da ação dos géis clareadores que contêm peróxido de carbamida na microdureza do esmalte dentário, procedeu-se da seguinte forma:
1. Seleção dos dentes e preparo dos corpos de prova:
Foram utilizados 25 incisivos centrais superiores humanos recém-extraídos, sem cáries na superfície vestibular e conservados em água destilada deionizada a 9 graus centígrados até o momento do uso. Esses dentes foram seccionados na junção esmalte-cemento, suas coroas foram separadas para o experimento e as raízes desprezadas.
As superfícies palatinas das coroas desses dentes foram removidas por meio de brocas diamantadas acionadas por motor de alta rotação com refrigeração a água. As superfícies vestibulares foram separadas e lavadas em água destilada deionizada a fim de remover quaisquer detritos que pudessem a ela ter aderido.
A seguir, essas superfícies coronárias vestibulares foram recortadas com disco de aço de dupla face, acionado por micromotor em baixa rotação, de modo a formar blocos retangulares. A porção recortada correspondia sempre à área central da superfície coronária vestibular, de forma a se obter prismas de esmalte com as mesmas inclinações. Cumpre salientar que, durante o corte, o disco era refrigerado com água corrente para evitar a queima do tecido dental.
Esses blocos eram, então, novamente lavados em água destilada deionizada e secos com lenços de papel absorvente. A seguir, eles eram incluídos em discos de acrílico de rápida polimerização, previamente preparados, de modo que a face vestibular (esmalte) ficasse exposta para o meio ambiente e a parte de dentina, no interior do disco de acrílico (Figura 1).
Após a polimerização do acrílico, a superfície do esmalte era lixada com lixas d'água de granulações 400, 500 e 600, sucessivamente, sob água corrente, a fim de que ficasse planificada. Em seguida, o esmalte era polido em uma politriz (Struers-Dinamarca) dotada de disco de feltro (Figura 2), associada a uma pasta de alumínio (Alpha Micropolishâ 10- Union Carbide).
O polimento da superfície de esmalte era controlado pelo exame visual em uma lupa, com aumento de 30X. O polimento só era considerado adequado à realização do teste de microdureza quando a superfície do esmalte apresentava-se sem riscos ou irregularidades, condição essencial para a visualização nítida das mossas produzidas pela máquina de dureza Vickers.
Figura 1. Bloco da superfície vestibular da coroa dental, incluída em disco de acrílico, com a face vestibular exposta
Figura 2. Politriz (Struers), dotada de disco de feltro para polimento
2. Produtos testados:
A escolha dos géis à base de peróxido de carbamida testados neste experimento foi feita de acordo com sua disponibilidade no mercado. Foram avaliados cinco produtos comerciais.
A
Tabela I lista os produtos testados, bem como suas composições
químicas, nomes dos fabricantes e procedências.
|
|
|||
| Nome comercial |
|
|
|
| Nite White® 16% | Peróxido de carbamida 16%; Glicerina; Carbopol; Sabor hortelã ou cereja. |
|
Beverly Hills, CA, USA |
| Nite White® 10% | Peróxido
de carbamida 10%;
Glicerina; Carbopol; Sabor hortelã ou cereja. |
|
Beverly Hills, CA, USA |
| Karisma Alpha® | Peróxido
de carbamida 10%;
Glicerina; Carbopol; Sabor hortelã. |
|
Louisville, CO, USA |
| Opalescence® | Peróxido
de carbamida 10%;
Glicerina; Carbopol; Sabor hortelã ou cereja. |
|
South Jordan, Utah, USA |
| Perfect Smile® * | Peróxido de carbamida; Glicerina; Água destilada; Carbopol; Trietanolamina; EDTA dissódico; Benzoato de sódio; Sorbato de potássio; Ácido cítrico; Sabor menta |
|
Natick, MA, USA |
| ®
= Marca registrada;
* = O fabricante não informa a concentração do peróxido de carbamida. Obs.: As bulas dos produtos testados encontram-se no Apêndice. |
|||
A Figura 3 mostra as formas de embalagem dos géis clareadores testados neste experimento.
Figura
3. Formas de embalagem dos géis clareadores testados: A) Nite
Whiteâ 16%; B) Nite Whiteâ 10%; C) Opalescenceâ ; D)
Karisma Alphaâ e E) Perfect Smileâ
3 - Aplicação dos géis clareadores:
Após seu preparo, os 25 corpos de prova foram divididos aleatoriamente em cinco (05) grupos experimentais, correspondendo aos cinco (05) produtos a serem testados. Os corpos de prova eram, então, imersos em um meio contendo saliva artificial por 24 horas. Decorrido este tempo, leu-se a primeira medida da microdureza do esmalte, que correspondia à microdureza normal do tecido testado.
A
solução mimetizante de saliva (saliva artificial) empregada
neste experimento foi aviada pela Faculdade de Ciências Farmacêuticas
de Ribeirão Preto - USP e sua composição química
está descrita na Tabela II.
| TABELA II. Composição da saliva artificial. | |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Com o emprego de um aparelho termoplastificador à vácuo, foram confeccionadas moldeiras de plástico termoformável que adaptavam-se aos discos de acrílico (corpos de prova). No interior dessas moldeiras, em sua parte central, soldou-se um disco graduado com capacidade de 0,2 ml, com a finalidade de acondicionar sempre a mesma quantidade do agente clareador. No momento em que a moldeira era adaptada ao corpo de prova, o gel testado entrava em contato com o esmalte incluído no disco de resina (Figura 4).
Figura
4. Moldeiras plásticas dotadas de recipiente para acondicionamento
de
0,2
ml de gel clareador: A) isolada e B) em posição no corpo
de prova
O conjunto corpo de prova/moldeira contendo o gel clareador era colocado em uma estufa a 37 graus centígrados e umidade relativa de 95 %. Essa umidade era fornecida pelo meio líquido de saliva artificial.
Decorridas 08 horas, os corpos de prova eram removidos da estufa e lavados em água destilada e deionizada por cinco minutos a fim de remover o máximo possível do gel clareador. Logo após, eles eram imersos em saliva artificial a 37 graus centígrados por 16 horas.
Após decorrido esse espaço de tempo, o gel clareador era novamente colocado sobre o esmalte e todo o ciclo era repetido por sete dias, com o intuito de simular um tratamento clareador caseiro.
Concluído o tempo experimental estipulado, mediu-se a microdureza do esmalte.
4 - Leitura da microdureza Vickers:
Para medir a microdureza Vickers do esmalte, utilizou-se um aparelho da marca Wolpert, de procedência alemã (Figura 5).
Os corpos de prova eram retirados da solução de saliva artificial, lavados em água destilada deionizada por um minuto e secos com gaze.
Em seguida, eram levados ao aparelho de medição e fixados sempre na mesma posição. Para que isto fosse possível, confeccionou-se um dispositivo de plástico dotado de vários pontos referenciais, que deveriam coincidir com os pontos marcados na mesa do aparelho.
A carga aplicada foi de 200 gramas durante 15 segundos. Essa carga e esse tempo foram estabelecidos após um cuidadoso estudo piloto, onde se verificou que eram suficientes para que a ponta de diamante do aparelho de microdureza penetrasse no esmalte dental e imprimisse uma mossa visível, como pode ser visto na Figura 6.
Figura 5. Aparelho para medida da microdureza Vickers (Wolpert-Alemanha)
Figura 6. Fotomicrografia do esmalte evidenciando uma mossa formada pela aplicação da carga de 200 gramas por 15 segundos
O comprimento das diagonais dessas mossas era anotado e, a seguir, transformado em dureza Vickers, segundo uma tabela de transformação fornecida pelo fabricante do aparelho. Quanto maior for o comprimento das diagonais, tanto menor a microdureza da dentina.
A
tabela de transformação utilizada para a dureza Vickers baseia-se
na fórmula:
![]()
Onde: P é a carga aplicada (200 gramas) e d a medida da diagonal das mossas elevada ao quadrado.
Procedeu-se do mesmo modo em todos os grupos testados. Obtiveram-se dez (10) medidas em cada corpo de prova antes e 10 medidas após o período experimental de aplicação dos géis clareadores sobre a superfície de esmalte.
As medidas da microdureza foram tomadas de forma que ficassem dispostas em duas fileiras paralelas, uma com as medidas do esmalte normal, anterior à aplicação dos géis clareadores e a outra, com as medidas obtidas no esmalte após submetido à ação desses agentes clareadores no tempo experimental.
A Figura 7 ilustra a disposição pareada das mossas, antes e após a aplicação dos géis clareadores.
Com
os resultados da microdureza do esmalte antes e após a aplicação
dos géis clareadores, procedeu-se à análise dos resultados.
Os 25 corpos de prova forneceram 500 leituras de microdureza que podem
ser vistas no Apêndice e na
Tabela
III.
Os
dados experimentais desse trabalho consistiram em 500 valores numéricos
resultantes das medidas da microdureza do esmalte humano (dureza Vickers)
dos dentes estudados. Esse número total de dados resulta do produto
fatorial de 25 dentes (superfície de esmalte), 10 medidas de cada
superfície analisada e 2 tempos (antes e após a aplicação
das soluções clareadoras): 25 x 10 x 2 = 500 (Tabela III).
|
|
||||||||||
| Soluções |
|
|||||||||
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Nite Whiteâ 10% |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Nite Whiteâ 16% |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Opalescenceâ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Karisma Alphaâ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Perfect Smileâ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Testes preliminares foram realizados, utilizando os dados originais da Tabela III e um software estatístico, elaborado pelo Prof. Dr. Geraldo Maia Campos, do Departamento de Estomatologia da FORP-USP (GMC software, versão 6.5), com a finalidade de verificar a normalidade da distribuição amostral, a fim de decidir sobre que tipo de estatística deveria ser empregada, paramétrica ou não-paramétrica.
Para se chegar a um resultado, foram necessárias cinco etapas, nas quais se calculavam os parâmetros amostrais, fazia-se a distribuição das freqüências acumuladas das curvas experimental e normal matemática, além de traçar o histograma de freqüências em intervalo de classe medidos pelo desvio padrão da amostra e verificar a homoscedasticidade amostral pelo teste de Cochran. Esses testes serão expostos a seguir:
1. Parâmetros amostrais
Pela
Tabela IV, observa-se que houve uma quantidade considerável de valores
situados no intervalo de classe a que pertence à média amostral,
e uma quase simetria da distribuição dos dados em torno da
média (135 dados abaixo contra 126 acima da média). Esses
parâmetros falam em favor de uma distribuição normal.
| TABELA IV. | Parâmetros amostrais dos dados originais. | |
| Variação total | 102202,0859 | |
| Variância da amostra | 204,8138 | |
| Desvio padrão da amostra | 14,3113 | |
| Erro padrão da média | 0,6400 | |
| Mediana (dados agrupados) | - 0,2695 | |
| Dados abaixo da média | 135 | |
| Dados iguais à média | 239 | |
| Dados acima da média | 126 | |
2. Distribuição das freqüências.
A Tabela V mostra que a distribuição das freqüências absolutas por intervalo de classe apresentam uma tendência central: 04, 25, 106, 239, 85, 38, 03.
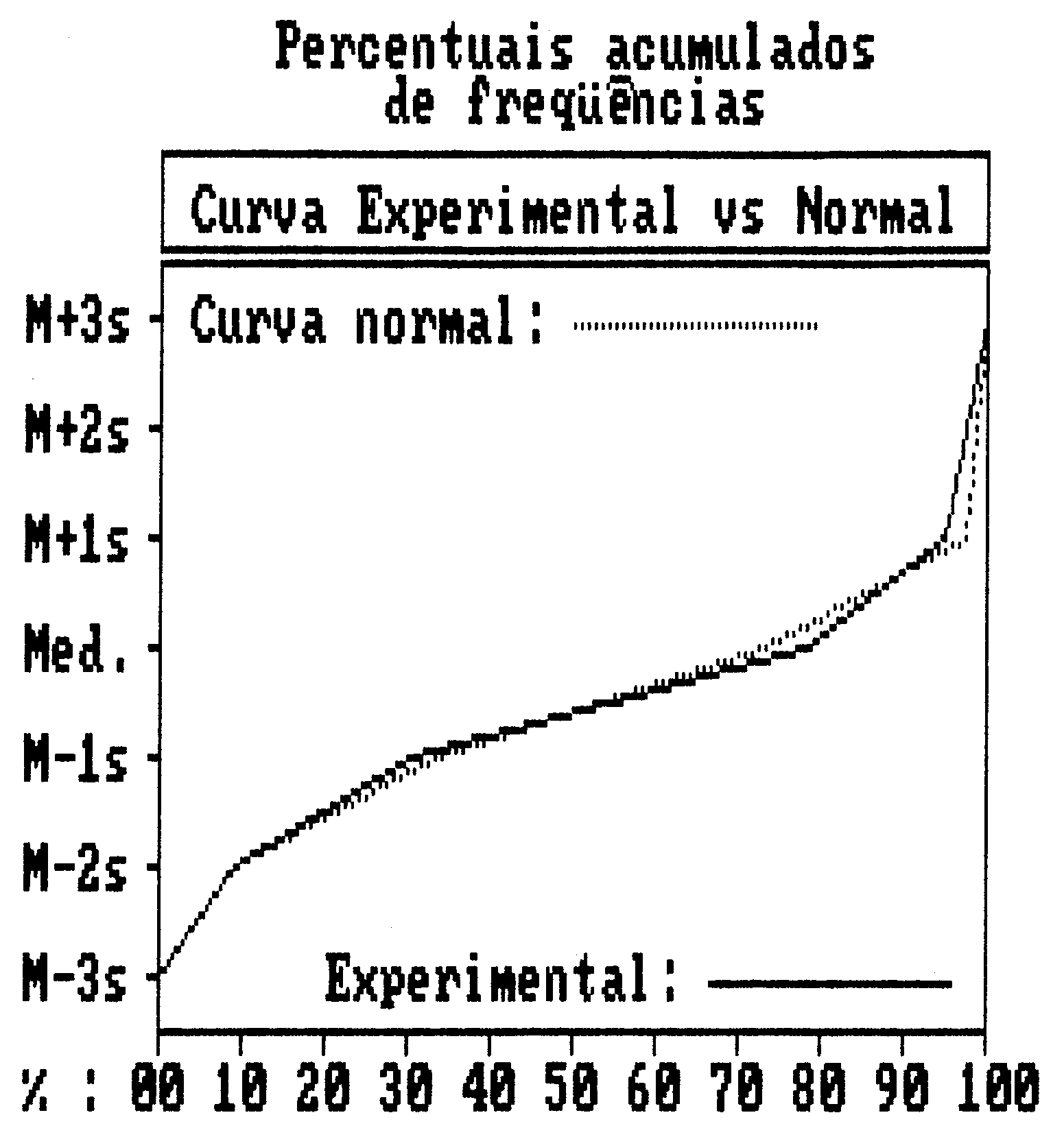
O gráfico da Figura 8 foi traçado a partir dos percentuais acumulados de freqüências, que constam na Tabela V.
Esse gráfico registra duas linhas superpostas, uma correspondente à curva normal matemática e a outra à curva experimental.
O
grau de concordância, de ajuste, ou de aderência entre essas
duas curvas é avaliado pela maneira como ambas se ajustam. A discrepância
relativamente pequenas entre elas traduz uma boa possibilidade da distribuição
amostral ser normal.
|
|
|||||||
| A. Freqüência por intervalo de classe | |||||||
| Intervalos de classe: |
|
|
|
|
|
|
|
| Freqüências absolutas: |
|
|
|
|
|
|
|
| Freqüências percentuais: |
|
|
|
|
|
|
|
| B. Freqüências acumuladas: | |||||||
| Intervalos de classe: |
|
|
|
|
|
|
|
| Freqüências absolutas: |
|
|
|
|
|
|
|
| Freqüências percentuais: |
|
|
|
|
|
|
|
 |
|
|
3. Teste de aderência à curva normal.
A
Tabela VI apresenta os resultados do teste de aderência da distribuição
de freqüências por intervalos de classe da distribuição
normal em relação à mesma distribuição
dos dados amostrais. Verifica-se que a probabilidade da distribuição
experimental ser normal é de 28,64 %.
|
|
||||||||
| A. Freqüência por intervalo de classe | ||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
24,20 | 39,89 | 24,20 | 5,40 | 0,44 | |
|
|
|
|
21,20 | 47,80 | 17,00 | 7,60 | 0,60 | |
| B. Cálculo do Qui quadrado | ||||||||
|
|
|
|
||||||
|
|
|
|
||||||
|
|
|
|||||||
4. Histograma de freqüência.
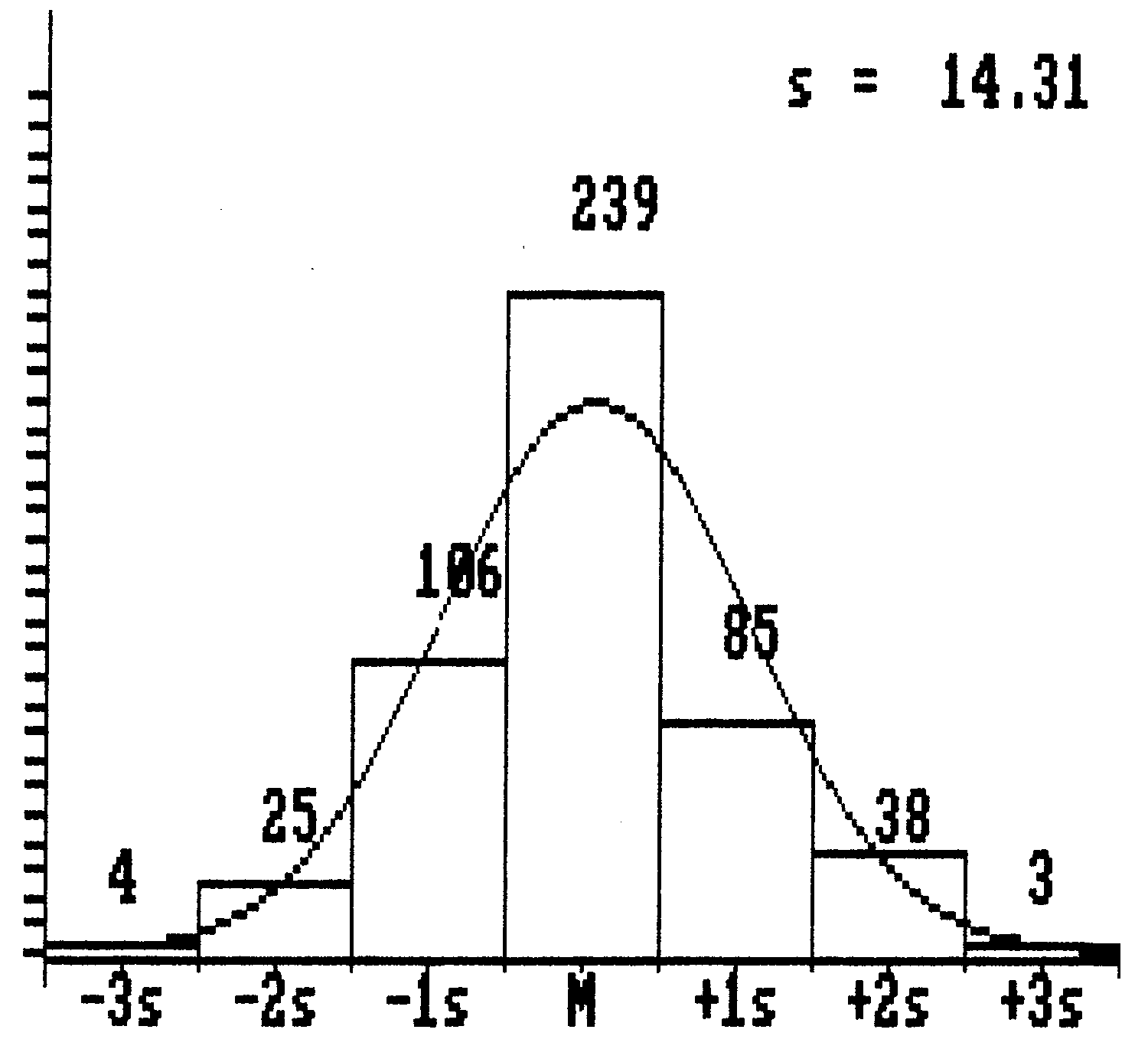
A
Figura 9 mostra o histograma de freqüências e curva normal dos
dados originais. Nessa figura, observa-se a distribuição
central dos dados experimentais e uma certa simetria em relação
à média, com números mais ou menos equivalentes abaixo
e acima dela. Uma distribuição que pode ser aceita como normal
para fins estatísticos.
 |
|
|
5. Teste de homogeneidade de Cochran.
Este teste compara a maior variância, individualmente considerada, contra a soma de todas as variâncias envolvidas nas amostras.
O valor calculado resulta da divisão da variância do maior valor pela soma de todas as variâncias utilizadas no estudo estatístico (DIXON & MASSEY Jr., 1969).
O valor crítico tabelado para 10 variâncias com 49 graus de liberdade é de 0,1811 para o nível de 1 por cento de significância. O teste realizado apresentou um valor calculado de 0,1948, que é ligeiramente maior e isso indica que as amostras não são perfeitamente homogêneas.
A análise do conjunto de resultados obtidos nesses testes preliminares levou à conclusão de que a distribuição amostral era normal, o que autorizava a aplicação de estatística paramétrica.
O teste paramétrico que melhor se adaptava ao modelo experimental era a análise de variância e, pelo fato de se tratar de um modelo misto, em que se associava ao mesmo tempo fatores de variação independentes (soluções clareadoras em forma de gel) e fatores de variação vinculados (dente - superfície do esmalte que tinha sua dureza medida antes e após a aplicação do agente clareador) usou-se o tipo de análise de variância do bloco partido.
Os
resultados podem ser vistos na Tabela VII, que é a análise
de variância no estilo tabela trincada ou bloco partido.
| TABELA VII. Analise de variância (Valores originais). | |||||
| Fonte de variação |
quadrados |
|
médios |
|
|
| Entre Tempos | 124916,4297 |
|
124916,4297 |
|
|
| Resíduo I | 15447,1699 |
|
157,6242 | ||
| Entre Soluções | 46956,2383 |
|
11739,0596 |
|
|
| Interação Tempos X Soluções | 35093,8125 |
|
8773,4531 |
|
|
| Resíduo II | 86660,3516 |
|
221,0723 | ||
| Variação Total | 309074,0 |
|
|||
A análise de variância acusou alta significância, ao nível de 0,01 por cento de probabilidade para a hipótese de igualdade, entre os tempos, ou seja, há diferença estatisticamente significante entre a microdureza do esmalte antes e após a aplicação das soluções clareadoras utilizadas.
Quanto às soluções estudadas, a análise de variância também acusou alta significância ao nível de 1% de probabilidade para a hipótese de igualdade, mostrando haver diferenças relevantes entre as ações destas soluções.
6. Teste de Tukey.
A
fim de esclarecer quais soluções testadas envolvidas na análise
de variância seriam significantemente diferentes entre si, efetuou-se
um teste de Tukey complementar (Tabela VIII), para comparação
entre as médias.
| TABELA VIII. | Teste de Tukey: Comparação entre soluções. | ||
|
|
|
|
|
| Opalescenceâ |
|
||
| Nite Whiteâ 10% |
|
||
| Perfect Smileâ |
|
|
|
| Karismaâ |
|
||
| Nite Whiteâ 16% |
|
||
| Símbolos iguais junto às médias representam valores estatisticamente não diferentes | |||
O teste Tukey acusou que as soluções Nite Whiteâ 10% e Perfect Smile atuaram de modo estatisticamente semelhante.
No que diz respeito à interação entre as soluções testadas e o tempo (antes e depois), a análise de variância evidenciou alta significância ao nível de 1% de probabilidade para hipótese de igualdade, ou seja, as soluções atuaram sobre a microdureza do esmalte de modo diferente.
A
fim de esclarecer quais das soluções envolvidas seriam diferentes
entre si quanto à redução da microdureza do esmalte,
após o tempo experimental de sua aplicação, efetuou-se
um teste de Tukey complementar para comparação entre médias
(Tabela IX).
| TABELA IX. | Teste de Tukey: Interação Soluções x Tempo. | ||
|
|
|
|
|
| Opalescenceâ x Antes |
|
||
| Nite Whiteâ 10% x antes |
|
||
| Nite Whiteâ 16% x Antes |
|
||
| Perfect Smileâ x Antes |
|
||
| Karisma Alphaâ x Antes |
|
|
|
| Opalescenceâ x Depois |
|
||
| Perfect Smileâ x Depois |
|
||
| Nite Whiteâ 10% x Depois |
|
||
| Karisma Alphaâ x Depois |
|
||
| Nite Whiteâ 16% x Depois |
|
||
| Símbolos iguais juntos às médias representam valores estatisticamente não diferentes | |||
Pelo teste de Tukey da interação Soluções x Tempo, observa-se que a microdureza do esmalte antes de se aplicar os agentes clareadores não apresenta diferença estatística entre si.
A aplicação dos agentes clareadores reduziu a microdureza do esmalte após o tempo experimental em todos os casos.
Os géis das marcas Perfect Smileâ , Nite Whiteâ 10% e Karisma Alphaâ reduziram a microdureza do esmalte de modo estatisticamente semelhante.
O gel da marca Opalescenceâ foi o que apresentou menor efeito sobre a redução da microdureza do esmalte.
O gel que mais ação teve sobre a redução da microdureza do esmalte foi o da marca Nite Whiteâ 16%.
Os gráficos das Figura 10 e 11 ilustram de modo mais claro a redução da microdureza do esmalte após a aplicação dos agentes clareadores no tempo experimental.
Figura 10 Interações da Soluções X Tempo (antes e depois) sobre a microdureza do esmalte. Dureza Vickers
Figura 11Valores médios da microdureza do esmalte antes e depois á aplicação do géis contendo peróxido de carbamida, no tempo experimental.
7. Teste de Wilcoxon.
Não obstante a análise estatística paramétrica ter sido autorizada pela análise
dos parâmetros amostrais, aplicou-se também a análise estatística não-paramétrica (Teste de Wilcoxon) para confirmar os resultados, dada a existência de um fator desfavorável, apontado pelo estudo da normalidade amostral, que era o fato das variáveis serem todas homogêneas.
O teste de Wilcoxon foi utilizado para comparar várias amostras com fatores de variação vinculados, ou seja, no mesmo corpo de prova avaliou-se microdureza antes e após a aplicação dos agentes clareadores.
Em primeiro lugar, aplicou-se o teste da microdureza para avaliar se havia diferença entre os valores da microdureza do esmalte antes e após do tratamento.
O teste de Wilcoxon indica que a diferença entre a microdureza antes e após o tratamento com os géis clareadores era significante ao nível de 1%.
Para
verificar o comportamento de cada solução sobre a microdureza
do esmalte, aplicou-se o Teste de Wilcoxon aos valores de microdureza antes
e após o tratamento (Tabela X).
|
|
|
|
|
|
| Opalescenceâ |
|
| Nite Whiteâ 10% |
|
| Nite Whiteâ 16% |
|
| Karisma Alphaâ |
|
| Perfect Smileâ |
|
| * Significante ao nível de 1%. | |
O
Teste de Wilcoxon confirma os achados do teste paramétrico, ou seja,
há significância estatística ao nível de 1%
entre a microdureza do esmalte antes e após o tratamento com os
géis clareadores testados e, ainda, que todos os géis comportaram-se
do mesmo modo, ou seja, reduzindo a microdureza do esmalte.
A utilização de agentes clareadores dentais caseiros tem aumentado de modo acentuado por vários motivos: a) é uma alternativa conservadora; b) os agentes podem ser auto-administrados pelo paciente, sob a orientação do profissional; c) é um procedimento cômodo para o cirurgião-dentista, possibilitando um menor número de sessões clínicas; d) é econômico; e) é muito difundida pela mídia.
Esses géis clareadores têm como agente ativo o peróxido de carbamida, que apresenta vários sinônimos, tais como: peró xido de uréia, peridrol-uréia, peróxido de hidrogênio carbamida, hyperol e pehydrit. Sua fórmula pode ser escrita dos seguintes modos: CH6N2O3 ou CO(NH2)2.H2O2. Seu peso molecular é de 94,07, tendo 12,77% de carbono, 6,43% de hidrogênio, 51,02% de oxigênio e 29,78% de nitrogênio. Usualmente, este produto contém 34-35% de H2O2. Apresenta-se na forma de um pó branco e cristalino, que decompõem-se no ar em uréia, oxigênio e água . É solúvel em água e decompõe-se em H2O2 e uréia (MERCK INDEX, 9674).
Empregou-se, neste trabalho, o vocábulo clareamento (s.m.) uma vez que o mesmo está devidamente expresso no Vocabulário Ortográfico da Língua Portuguesa - Academia Brasileira de Letras (1981). Tomamos o cuidado de seguir essa indicação, uma vez que o Dicionário Aurélio Eletrônico o traz como vocábulo inexistente.
Cumpre salientar que, para a realização do presente trabalho de investigação da microdureza do esmalte sob ação de agentes clareadores à base de peróxido de carbamida em forma de gel, fazia-se necessário saber qual a carga que deveria ser aplicada ao diamante do aparelho que mede a dureza Vickers.
Assim, para estabelecer qual a carga ideal para produzir uma mossa nítida e capaz de marcar a estrutura de esmalte, realizou-se um estudo piloto. Os trabalhos de PÉCORA et al (1994), e FAIRBANKS (1995) mediram a microdureza da dentina com carga de 50 gramas por 15 segundos. Desse modo, a partir dessa carga de 50 gramas, realizaram-se várias medidas com carga incrementada de 10 em 10 gramas até se obter uma mossa perfeita, nítida e de fácil leitura. Após esse teste piloto, concluiu-se que a carga de 200 gramas era suficiente para que o diamante da máquina de dureza deixasse uma mossa nítida e mensurável (Figura 6) na superfície do esmalte humano. Assim, padronizou-se a aplicação desta carga por um tempo de 15 segundos em todos os corpos de provas.
Os dados da microdureza, 250 obtidos antes da aplicação dos géis clareadores nos corpos de prova e 250 após as suas aplicações por um período experimental de sete dias, na tentativa de simular o que ocorre na cavidade bucal durante um tratamento clareador, foram utilizados para o tratamento estatístico.
Esses 500 dados foram utilizados na realização de testes preliminares para se verificar a normalidade da distribuição amostral, a fim de estabelecer o melhor tipo de estatística a ser empregada. Não foi utilizada nenhuma média das medidas, uma vez que os dados da microdureza do esmalte antes e após o tratamento são dados vinculados, ou seja, dados obtidos nos mesmos corpos de prova.
Os testes preliminares permitiram a aplicação da análise estatística paramétrica com a ressalva de uma pequena homogeneidade da amostra, fato este esperado, uma vez que a dureza do esmalte pode variar de pessoa para pessoa. Esta variação individual deve ser levada em consideração por ser uma característica humana.
Assim, para abranger todas as possibilidades estatísticas, realizamos o teste de variância em forma de bloco partido, no qual se podia avaliar os fatores de variação vinculados (tempo - antes e depois) e os fatores independentes (géis clareadores utilizados), e também o teste estatístico não-paramétrico de Wilcoxon. Este último teste tem a finalidade de avaliar múltiplos fatores, sendo pelo menos um deles vinculados.
De modo claro, os dois tratamentos estatísticos apontaram os mesmos resultados, o que expressou a fidelidade dos dados experimentais.
A Tabela V ilustra a análise de variância no estilo tabela trincada ou bloco partido e expressa que a diferença entre microdureza do esmalte antes (normal) e após a aplicação dos géis clareadores é estatisticamente significante ao nível de 1%, o que significa redução marcante da microdureza do esmalte dental humano após aplicação desses géis.
O exame da análise de variância também indicou que todas as soluções empregadas (géis) atuaram sobre a microdureza do esmalte de modo estatisticamente diferente entre si, ao nível de 1%.
A fim de esclarecer quais das soluções testadas envolvidas seriam significantemente diferentes entre si, ou seja, como elas se comportavam, aplicou-se o teste de Tukey complementar (Tabela VI). Esse teste indicou que o gel Nite Whiteâ 16% foi o que mais reduziu a microdureza no tempo experimental; o Opalescenceâ o que menos reduziu e que o Nite Whiteâ 10% e o Perfect Smileâ reduziram a microdureza de modo semelhante entre si.
Assim, podemos ordenar os géis clareadores do que mais reduziu a microdureza do esmalte para o que menos reduziu: 1o Nite Whiteâ 16%; 2o Karisma Alphaâ ; 3o Perfect Smileâ e Nite Whiteâ 10% e, por último, o Opalescenceâ .
Os gráficos 10 e 11 ilustram de forma bem clara os resultados estatísticos obtidos.
A aplicação do teste não-paramétrico de Wilcoxon forneceu os mesmos resultados dos testes paramétricos.
Os géis clareadores para dentes vitais mais correntemente utilizados apresentam em sua fórmula o peróxido de carbamida como agente ativo e o carbopol como veículo.
O carbopol (carboxipolimetileno) é um polímero de vinil em forma de pó branco e que, ao se misturar com a água forma um gel rico em ions e ligeiramente ácido. Esse produto é empregado como agente dispersante, emulsionante e lubrificante, favorecendo uma melhor aderência do agente clareador aos tecidos e o retardamento da liberação de oxigênio.
Nota-se que, na composição química do Perfect Smileâ , há os seguintes produtos: glicerina, peróxido de carbamida, água destilada, carbopol, trietanolamina, EDTA sal dissódico, benzoato de sódio, ácido cítrico, sabor hortelã e adoçante artificial. Com base nesta composição química, pode-se extrapolar que o carbopol, a glicerina , a trietanolamina entram como agentes espessantes e emulsionantes. O peróxido de carbamida atua como componente ativo liberador de peróxido de hidrogênio e uréia, que, por sua vez, também sofrem desdobramento: o peróxido de hidrogênio libera oxigênio nascente e ions hidroxila e a uréia se decompõe em gás carbônico e água. O EDTA sal dissódico é um muito conhecido agente quelante, que foi introduzido nos tratamentos de canais radiculares atrésicos por Æ STBY (1957). O benzoato de sódio é um agente conservante e a sua função é evitar que os componentes orgânicos se decomponham. O ácido cítrico, provavelmente, está aí colocado para formar um meio ligeiramente ácido, com o objetivo de retardar a quebra da molécula do peróxido de carbamida.
Sabe-se que os peróxidos, tanto de hidrogênio quanto o de carbamida, liberam lentamente oxigênio em meio ácido. Para obter essa liberação lenta, os fabricantes devem fornecer ao produto um meio ácido ou, pelo menos, ligeiramente ácido.
O fabricante do produto Perfect Smileâ parece fornecer uma fórmula mais fidedigna, uma vez que evidencia a presença do EDTA, do ácido cítrico e de um conservante (benzoato de sódio). Os demais fabricantes dos géis testados no presente trabalho informam uma composição química (Tabela I) cuja realidade pode ser colocada em dúvida, pois mencionam apenas o agente ativo, o carbopol e o flavorizante. Eles não citam o próprio conservante utilizado, sem o qual esses produtos orgânicos poderiam ser contaminados por bactérias e fungos.
Assim, sem um agente conservante e sem um meio ácido, os produtos teriam um shelf life extremamente curto, invibiabilizando sua comercialização.
Todos os agentes clareadores para dentes vitais recentemente introduzidos no mercado contêm alguma forma de peróxido de hidrogênio, que apresenta a propriedade de gerar radicais livres. O peróxido de hidrogênio decompõe-se em solução aquosa fornecendo oxigênio nascente e radicais hidroxila altamente reativos. O radical livre tem falta de elétrons, sendo extremamente eletrofílico e instável e, assim, ataca a grande maioria de moléculas orgânicas para atingir a estabilidade. Os radicais eletrofílicos podem reagir facilmente com moléculas insaturadas resultando em mono ou di-hidroxilação. Os radicais livres gerados pelo peróxido de hidrogênio, ao interagirem com as moléculas das substâncias orgânicas escurecidas por reação de óxido-redução, dão novos compostos, de coloração diferente, mais clara. Por ser capaz de desencadear este mecanismo, o peróxido de hidrogênio é considerado um forte agente clareador.
Cumpre informar que FEIMAN (1991) salientou que a FDA (Food and Drugs Administration) liberou o uso do peróxido de carbamida e do peróxido de hidrogênio a 3% como antissépticos bucais e FRISH (1995) informou que a ADA (American Dental Association), em seu último relatório, citou os riscos potenciais do uso de produtos à base de peróxido de carbamida, reforçando a necessidade de mais investigações sobre esses produtos.
SCHERER et al (1991), SEGHI & DENRY (1992), BITTER (1992) e SHANNON et al (1993) ao estudarem a ação dos géis clareadores contendo peróxido de carbamida sobre a microdureza e a morfologia superficial do esmalte, verificaram que a superfície tornava-se rugosa, mas a microdureza não era alterada.
Neste trabalho, entretanto, verificou-se que a microdureza do esmalte é reduzida após a aplicação dos géis clareadores à base de peróxido de carbamida. A discrepância deste resultado com o dos demais pesquisadores provavelmente se deve ao fato de que eles utilizaram cargas excessivas para medir a microdureza do esmalte humano. SEGHI & DENRY (1992) utilizaram carga de 400 gramas e SHANNON et al (1993) utilizaram carga de 1000 gramas. Essas cargas são extremamente excessivas e mascaram quaisquer resultados.
Apontar o produto químico peróxido de carbamida, isoladamente, como responsável por alterar a microdureza do esmalte seria temerário. Acreditamos que a redução da microdureza do esmalte pode ser relacionada à soma de dois fatores: a) a ação do peróxido de carbamida sobre a matriz orgânica do esmalte (COVINGTON et al, 1992) e b)a ação de agentes ácidos ou quelantes presentes na composição dos géis clareadores à base de peróxido de carbamida.
A
realização deste trabalho induziu alguns raciocínios
que abrem campo para novas investigações a respeito da ação
dos agentes clareadores em forma de gel auto-administrados pelo paciente,
tais como: até que ponto a redução da microdureza
do esmalte favorece a sua fratura?; a mudança da microdureza favorece
o aumento da permeabilidade do esmalte?; e, finalmente, como obter um clareamento
de dente vital sem prejudicar as estruturas dentais?
Com base na metodologia empregada e na análise dos resultados obtidos com os produtos testados, pode-se concluir que:
1. O esmalte humano sofreu redução estatisticamente significante de sua microdureza após a aplicação de géis clareadores à base de peróxido de carbamida.
2.
O gel Opalescenceâ foi o que menos reduziu a microdureza do esmalte.
Os géis Perfect Smileâ , Nite Whiteâ 10% e o Karisma
Alphaâ reduziram a microdureza do esmalte de modo estatisticamente
semelhante entre si e o gel Nite Whiteâ 16% foi o que provocou a
maior redução da microdureza do esmalte.
Estudou-se
a ação de géis clareadores à base de peróxido
de carbamida sobre a microdureza do esmalte humano.
Utilizaram-se
25 incisivos centrais superiores recém extraídos. As superfícies
vestibulares das coroas desses dentes foram removidas e recortadas com
discos de aço dupla face de modo a formar blocos retangulares. Estes
blocos de esmalte foram incluídos em discos de acrílico previamente
preparados, de modo que a parte de esmalte ficasse exposta para o meio
ambiente e a parte de dentina, no interior do disco de resina acrílica.
Os discos foram divididos em grupos de cinco e, após a planificação
e polimento da superfície de esmalte, foram tomadas dez medidas
de microdureza em cada corpo de prova. Os cinco grupos foram submetidos
à ação do peróxido de carbamida de 05 diferentes
marcas comerciais (Nite Wite? 16%; Nite White? 10%; Opalescence?; Karisma
Alpha? e Perfect Smile?), por 08 horas diárias, permanescendo em
estufa a 37º C e umidade relativa de 95%. Após um tempo experimental
de sete dias, foram tomadas novamente as medidas da microdureza. Para medir
a microdureza da dentina, utilizou-se um aparelho de dureza Vickers com
200 gramas de carga e 15 segundos de aplicação. O método
mostrou-se eficaz e reprodutível e a análise estatística
dos resultados demonstrou que todos os produtos testados reduziram de maneira
estatisticamente significante a microdureza do esmalte no tempo experimental
estipulado.
Unitermos:
Peróxido de carbamida, microdureza, agentes clareadores.
The effect of cabamide peroxide-based bleaching gels on the microhardness of human enamel was studied. Twenty-five recently-extracted maxillary central incisors were used. The buccal surfaces of the crowns of these teeth were removed and cut with double-faced steel disks to form rectangular blocks. These blocks of enamel were placed in previously prepared acrylic disks so that the enamel was exposed to the environment with the dentin on the inner part of the acrylic resin. The disks were divided into groups of 5 and after planing and polishing of the enamel surface, ten measurements of microhardness were taken for each sample. The five groups were submitted to five different brands of carbamide peroxide (16% Nite White?; 10% Nite White?; Opalescence?; Karisma Alpha? and Perfect Smile??? for 8 hours daily, at 37?C, 95% relative humidity. After 7 days, new microhardness measurements were taken using a Vickers hardness apparatus with 200 g for 15 seconds. Statistical analysis showed that the microhardness of the enamel was reduced significantly by all products.
Key
Words: Carbamide peroxide, microhardness, bleaching agents.
ABBOT, C.H. Bleaching discolored teeth by means of the 30 per cent perhidrol and electric light rays. Journal Allied Dental Society, v.13, n.3, p.259, 1918.
ACADEMIA BRASILEIRA DE LETRAS. Vocabulário Ortográfico da Língua Portuguesa. Rio de Janeiro, Bloch Editores, 1981. p.173.
AMES, J. Removing stains from mottled enamel. Journal of American Dental Association, v.24, n.10, p.1674-1677, October 1937.
ATKINSON, W.H. Bleaching teeth. The Dental Cosmos, v.6, n.11, p.597-599, June 1865.
AUN, C.E.; MOURA, A.A.M. Clareamento dental. In: PAIVA, J.G.; ANTONIAZZI, J.H. Endodontia: bases para a prática clínica. 2 ed. São Paulo, Artes Médicas, 1988. p. 759-777.
BARRIENTOS, P.; ABARCA, A.M.; FRANCO, M.E.; PESCE, H.F. Estudo de dentes com pigmentações intrínsecas. Revista Brasileira de Odontologia, v.51, n.5, p.43-47, setembro/outubro 1994.
BISHARA, S.E.; SULLEMAN, A.H.; OLSON, M. Effect of enamel bleaching on the bonding strenght of orthodontic brackets. American Journal of Orthodontics and Dentofacial Orthopedics, v.104, n.5, p.444-447, November 1993.
BITTER, N.C. A scanning electron microscopy study of the effect of bleaching agent on enamel: a preliminary report. Journal of Prosthetic Dentistry, v.67, n.6, p.852-855, June 1992.
BLECHMAN, H.; COHEN, M. Use of aqueous urea solution in the field of endodontic : preliminary report. Journal of Dental Research, v.30, n.4, p.503-504, August 1951.
BOGUE, E.A. Bleaching teeth. The Dental Cosmos, v.14, n.1, p.1-3, January 1872.
BOWLES, W.H.; THOMPSON, L.R. Vital bleachuing: the effects of heat and hydrogen peroxide on pulpar enzymes. Journal of Endodontics, v.12, n.3, p.108-112, March 1986.
BOWLES, W.H.; UGWUNERI, Z. Pup chamber penetration by hidrogen peroxide following vital bleaching procedures. Journal of Endodontics, v.13, n.8, p.375-377, August 1987.
BOWLES, W.L. ; BURNS, Jr.H. Catalase/peroxidase activity in dental pulp. Journal of Endodontics, v.18, n.11, p.527-529, November 1992.
BUCKLEY, J.P. Causas y tratamiento de la decoloración dentaria. In: JOHNSON, C.N.: La Práctica Odontológica, 4 ed. Barcelona - Buenos Aires, Editorial Labor, 1927. p.365-374.
BUCKLEY, J.P. Materia Medica, Farmacologia y Terapeutica Clínica Dental Modernas. 4 ed. Barcelona - Buenos Aires, Editorial Labor, 1926. p.339-347.
CANEPA, R.; SOUZA NETO, M.M.; SAQUY, P.C.; ROMANI, N.F.; PÉCORA, J.D. Estudo in vitro da ação do agente clareador (perborato de sódio + peróxido de hidrogênio + calor) sobre a microdureza da dentina. Revista Paulista de Odontologia, v.15, n.4, p.18-24, julho/agosto 1993.
CHARPLE, J.A. Restorating discolored teeth to normal. The Dental Cosmos, v.19, n.9, p.499, September 1877.
CHERRY, D.V.; BOWERS, Jr, D.E.; THOMAS, L.; REDMON, A.F. Acute toxicological effects of ingested tooth whiteners in female rats. Journal of Dental Research, v.72, n.9, p.1298-1303, September 1993.
CHRISTENSEN, G.J. To bleach or not to bleach? Journal of American Dental Association, v.122, n.12, p.64-65, December 1991.
COBE, H.M. Investigations of a new dental chemotherapeutic agent in the presence of blood. Oral Surgery, v.13, n.1, p.678-685, June 1960.
COHEN, S.; CHASE, C. Human pulpar response to bleaching procedures on vital teeth. Journal of Endodontics, v.5, n.5, p.134-138, May 1979.
COOPER, J.S.; BOKMEYER, J.B.; BOWLES, W. penetration of the pulp chamber by carbamide peroxide bleaching agents. Journal of Endodontics, v.18, n.7, p.315-317, July 1992.
CORCORAN, J.F.; ZILLICH, A.R.M. Bleaching of vital tetracycline stained teeth. Journal of Michigan Dental Association, v.56, p.340-343, 1976.
COVINGTON, J.S.; FRIEND, G.W.; LAMOREAUX, W.J. Carbamide peroxide tooth bleaching: effects on enamel composition and topography. Journal of Dental Research, v.69, p.175, 1990. [Abstract of Papers. abstract 530.].
CURTIS Jr.,J.W.; DICKINSON, G.L.; MYERS, M.L.; RUSSEL, C.M. Evaluating the effects of a dentist-supervised, pacient-applied carbamide peroxide bleaching agent on oral soft tissues. Journal of Esthetic Dentistry, v.7, n.1, p.18-25, January 1995.
DAHL, J.E.; BECHER, R. Acute toxicity of carbamide peroxide and a commercially available tooth-bleaching agents in rats. Journal of Dental Research, v.74, n.2, p.710-714, February 1995.
DAHLSTRON, S.W. Hydroxy radical activity in bleached root filled teeth. Australian Endodontic Newsletter, v.19, n.1;.p.30-31, August 1993.
DALE, B.G. Esthetic Dentistry: a clinical approach to techniques and materials. Pensylvania Lea & Febiger, 1993. p.205-225.
DIXON, W.J.; MASSEY Jr., F.H. Introduction to statistical analysis. 4 ed., São Paulo, McGraw-Hill, 1969.
EISENBERG, E.; BERNICK, S.M. Anomalies of the teeth with stains and discolorations. Journal of Preventive Dentistry, v.2, n.1, p.7-20, January/February 1975.
FAIRBANKS, D.C.O. Avaliação da capacidade quelante do EDTA, do EDTAC e do EDTA-T pela análise da microdureza da dentina radicular. Rio de Janeiro, 1995.82p. Dissertação (Mestrado) - Faculdade de Odontologia da Universidade do Estado do Rio de Janeiro.
FEINMAN, R.A.; MADRAY, G.; YARBOROUGT, D. Chemical, optical, and physiologic mechanism of bleaching products: a review. Practice Periodontology Aesthetic, v.3, p.32-36, 1991.
FRANK, A.L. Branqueamento de dentes pulpados e despulpados. In: COHEN, S.; BURNS, R.C. Caminhos da Polpa, 2 ed traduzida por Sylvio Bevilacqua. Rio de Janeiro, Guanabara Koogan, 1982. p.541-547.
FRIEDMAN, S.; ROTSTEIN, I.; LIBFELD, H.; STABHOLZ, A.; HELING, I. Incidence of external root resorption and esthetic results in 59 bleached pulpless teeth. Endodontics Dental Traumatology, v.4, n.1, p.23-26, January 1988.
FRYSH, H.; BOWLES, ,W.H.; BAKER, F.; RIVERA-HIDALGO, F.; GUILLEN, G. Effect of pH on hydrogen peroxide bleaching agents. Journal of Esthetic Dentistry, v.7, n.3, p.130-133, March 1995.
GIBSON, A. E. The treatment of discolored teeth. The Dental Cosmos, v.52, n.10, p.932-933, October 1910.
GLICKMAN, G.N.; FRYSH, H.; BAKER, F.L. Adverse response to vital bleaching. Journal of Endodontics, v.18, n.7, p.351`-354, July 1992.
GOON, W.W.Y.; COHEN, S.; BORER, R. External cervical root resorption following bleaching. Journal of Endodontics, v.12, n.9, p.414-418, September 1986.
GROSSMAN, L.I. Root Canal Therapy. 2 ed. Philadelphia, Lea & Febiger, 1946.
HALL, D.A. Should etching be performed as a part of vital bleaching technique? Quintessence International, v.22, n.9, p.679-686, September 1991.
HARLAN, A.W. The removal of stains from the teeth caused by administration of medicinal agents and bleachinh of pulpless teeth. American Dental Journal, v.18, n.5, p 521, 1884.
HARRINGTON, G.W.; NATKIN, E. External resorption associated with bleaching of pulpless teeth. Journal of Endodontics, v.5, n.11, p.344-347, November 1979.
HAYWOOD, V.B. Commonly asked question about Nightguard vital bleaching. IDA Journal, n.5, p.28-33, September/October 1993.
HAYWOOD, V.B. History, safety, and effectiveness of current bleaching techniques and applications of the nightguard vital bleaching technique. Quintessence International, v.23, n. 7, p.471-488, July 1992.
HAYWOOD, V.B.; HEYMANN, H.O. Nightguard vital bleaching. Quintessence International, v.20, p.173-176, 1989.
HAYWOOD, V.B.; HEYMANN, H.O. Nightguard vital bleaching: how safe is it? Quintessence International, v.22, n.7, p.515-523, July 1991.
HAYWOOD, V.B.; LECH, T.; HEYMANN, H.O.; CRUMPLER, D.; BRUGGERS, K. Nightguard vital bleaching: effects on enamel texture and diffusion. Quintessence International, v.21, n.10, p. 801-804, October 1990.
HELLER, D.; SKRIBER, J.; LIN, L.M. Effect of intracoronal bleaching on external cervical root resorption. Journal of Endodontics, v.18, n.4, p.145-148, April 1992.
HOWELL, R.A. The prognosis of bleachead root-filled teeth. International Endodontic Journal, v.14, n.1, p. 22-26, January 1981.
JORDAN, R.E.; SUZUKI, M.; CROLL, T.P. Tratamiento conservador de las corolaciones anómalas de los dientes. In: Grabado Composto Estético, Barcelona, Grafos., 1994. p.84-132.
KERN, R. Iodin and calcium hypochlorite in abnormal discoloration of the teeth. The Dental Cosmos, v.52, n.2, p.374-375, February 1910.
KILLIAN, C.M. Conservative color improvement for teeth with fluorosis-type stain. Journal of American Dental Association, v.124, n.5, p.72-74, May 1993.
KIRK, E.C. Chemical principles involved in tooth discoloration. The Dental Cosmos, v.48, n.9, p.947-955, September 1906.
KIRK, E.C. Manuel de Dentisterie Operatóire, 3 ed. Paris, Masson Editeurs, 1910. p.501-524.
KIRK, E.C. Sodium peroxide (Na2O2): a new dental bleaching agent and antisseptic. The Dental Cosmos, v.35, n.2, p.192-198, February 1893.
KWONG, K; MOHAMMED, S.; McMILLIAN, M.; STOKES, A.N. Evaluation of a 10 percent carbamide peroxide gel vital bleaching agent. New Zeland Dental Journal, v.89, n.1, p. 18-22, January 1993.
LADO, E.A.; STANLEY, H.R.: WEISMAN, M.I. Cervical resorption in bleaching teeth. Oral Surgery, Oral Medical and Oral Pathology, v.55, n.1, p.78-80, January 1983.
LATCHAM, N.L. Postbleaching cervical resorption. Journal of Endodontics, v.12, n.6, p.262-264, June 1986.
LEVINH, P. Safety whiteners. Journal of Canadian Dental Association, v.57, n.12, p.925-926, December 1991.
MQUILLEN, J.H. Bleaching discolored teeth. The Dental Cosmos, v.8, n.9, p.457-459, September 1867.
MQUILLEN, J.H. Microscopy study of dental tissues. The Dental Cosmos, v.7, n.9, p.449-455, September 1866.
MQUILLEN, J.H. Review od dental literature and art: bleaching agents. The Dental Cosmos, v.3, n.4, p.205-206, April 1861.
MAISTO, O.A. Endodoncia. Buenos Aires, Editorial Mundi, 1967. p.341-344.
McEVOY, S.A. Chemical agents for removing intrinsic stains from vital teeth. II: Current techniques and their clinical aplication. Quintessence International, v.20, p.379-384, 1989.
McEVOY, S.A. Removing intrinsic stains from vital teeth by microabrasion and bleaching. Journal of Esthetic Dentistry, v.7, n.3, p.104-109, 1995.
MERCK INDEX: an encyclopedia of chemical, drugs and biologicals. 10 ed. Rahway, Merck, 1993. p.1410.
NATHANSON, D.; PARRA, C. Bleaching vital teeth: a review and clinical study. Copenhagen Contin. Education Dental, v.8, n.7, 479-497, July 1987.
NUTTING, E.B.; POE, G.E. A new combination for bleaching teeth. Journal S. Californian Dental Association, v.41, n.2, p.289-291, February 1963.
PAULA EDUARDO, C.; AUN, C.E. Clareamento de dentes vitalizados. Revista de Odontologia Unicid, v.5, n.1, p.27-34, janeiro/junho 1993.
PÉCORA, J.D., CRUZ FILHO, A.M.; SOUSA NETO, M.D.; SILVA, R.G. In vitro action of various bleaching agents on the microhardness of human dentin. Brazilian Dental Journal, v.5, n.2, p.129-134, 1994.
PÉCORA, J.D.; SOUSA NETO, M.D.; COSTA, W.F. Apresentação de um método químico que revela in vitro a passagem do peróxido de hidrogênio a 30 por cento através da dentina radicular. Revista Paulista de Odontologia, v.13, n.2, p.34-37, março/abril 1991.
POWELL, L.D.; BALES, J.D. Tooth bleaching: its effect on oral tissues. Journal of American Dental Association, v.122, n.11, p.50-53, November 1991.
PRINZ, H. Recent improvements in tooth bleaching: a clinical syllabus. The Dental Cosmos, v.66, n.6, p.558-560, June 1924.
RADETIC, E.A. Nova técnica de clareamento dos dentes despulpados. Rio de Janeiro, 1987. 42p. Dissertação (Mestrado) Faculdade de Odontologia da Universidade do Estado do Rio de Janeiro.
RITTER, A.V.; MACHADO, A.A.; BARATIÉRI, L.N.; VIEIRA, L.C.C. Técnica caseira para clareamento dos dentes vitais. Revista Gaúcha de Odontologia, v.40, n.5, p.363-367, 1992.
ROBERTSON, W.D.; MELFI, R.C. Pulpal response to vital bleaching procedures. Journal of Endodontics, v.6, n.7, p..645-649, July 1980.
ROTSTEIN, I. In vitro determination and quantification of 30% hydrogen peroxide penetration through dentin and cementum during bleaching. Oral Surgery, Oral Medical, Oral Pathology, v.72, n.5, p.602-606, November 1991.
ROTSTEIN, I.; LEHR, Z.; GEDALIA, I. Effect of bleaching agents on inorganic components of human dentin and cementum. Journal of Endodontics, v.18, n.6, p.290-293, June 1992.
ROTSTEIN, I.; MOR, C.; FRIEDMAN, S. Prognosis of intracoronal bleaching with sodium perborate preparations in vitro: 1 - year study. Journal of Endodontics, v.19, n.1, p.10-12, January 1993.
ROTSTEIN, I.; ZALKIND, M.; MOR, C.; TARABEACH, A.; FRIEDMAN, S. In vitro efficacy of sodium perborate preparations used for intracoronal bleaching of discolored non-vital teeth. Endodontics Dental Traumatology, v.7, p.177-180, 1991.
SALVAS, J.C. Perborate as a bleaching agent. Journal of American Dental Association, v.25, n.2, p.324, February 1938.
SAQUY, P.C.; SOUSA NETO, M.D., CANEPA, R.; PÉCORA, J.D. Estudo in vitro da permeabilidade dentinária após aplicação de agentes clareadores. Revista Paulista de Odontologia, v.14, p.37-40, 1992.
SCHERER, W.; COOPER, H.; ZIEGLER, B.; VIJAYARAGHAVAN, T.V. At home bleaching system: effects on enamel and cementum. Journal of Esthetic Dentistry, v.3, n.2, p. 54-56, March/April 1991.
SCHULTE, J.R.; MORRISSETE, D.B.; GASIOR, E.J. CZAJEWSKI, M.V. The effects of bleaching application time on the dental pulp. Journal of American Dental Association, v.125, n.10, p.1330-1335, October 1994.
SEALI, N.S.; MACINTOSHM, J.E.; TAYLOR, A.N. Pulpal reactions to bleaching of teeth dogs. Journal of Dental Research, v.60, p.948-953, 1981.
SEGHI, R.R.; DENRY, I. Effects of external bleaching on indentation and abrasion characteristics of human enamel in vitro. Journal of Dental Research, v.71, n.6, p.1340-1344, June 1992.
SHANNON, H.; SPENCER, P.; GROSS, K.; TIRA, D. Characterization of enamel exposed to 10% carbamide peroxide bleaching agents. Quintessence International, v.24, n.1, p.39-44, January 1993.
SPASSER, H.F. A simple bleaching technique using sodium perborate. New York State Dental Journal, v.27, n.7, p.332-334, August/September 1961.
STEWART, G.G.; COBE, H.M.; KAPSIMALAS, P. A study of a new medicament in the chemomechanical preparation in infected root canal. Journal of American Dental Association, v.62, n.2, p.33-37, July 1961.
STEWART, G.G.; KAPSIMALAS, P.; RAPPAPORT, H. EDTA and urea peroxide for root canal preparation. Journal of American Dental Association, v.78, n.2, p.335-338, February 1969.
SWIFT, E.J.A. A method for bleaching discolored vital teeth. Quintessence International, v.19, n.9, p.607-611, September 1988.
TITTLEY, K.C.; TORNECK, C.D.; SMITH, D.C. The effect of concentrated hydrogen peroxide solutions on the surface morphology of human tooth enamel. Journal of Endodontics, v.14, n.2, p.69-74, February 1988.
TONG, L.S.M.; PANG, M.K.M..; MOK, N.Y.C.; KING, N.M.; WEI, S.H.I. Effects of etching, micro-abrasion, and bleaching on surface enamel. Journal of Dental Research, v.72, n.1, p.67-71, January 1993.
TRUMAN, J. Bleaching teeth. The Dental Cosmos, v.23, n.6. p.281-288, June 1881.
VIEIRA, D.; ISHIDA, F.; FUKUSHI, M.; BARBOSA,,W.F.S. Técnica para clareamento homogêneo de dentes vitalizados manchados por tetraciclina. Âmbito Odontológico, v.7, p. 372-377, 1993.
WESTLAKE, A. Bleaching teeth by eletricy. American Journal Dental Science, v.29, p.101, 1895.
WONG, M.; SCHIMIDT, J.C. Vital bleach of hemorrhagic discoloration. Journal of Endodontics, v.17, n.5, p. 242-243, May 1991.
WOODNUTT,
C. Discoloration of dentine. The Dental Cosmos, v.2, n.12, p.662, July
1860.